
 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.回答有关中和反应的问题.
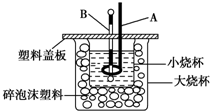
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.回答有关中和反应的问题.分析 (1)仪器A的名称是环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作;
(3)若保温效果不好,有热量散失,求得的中和热数值将会减小;
(4)根据弱电解质电离吸热分析;中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量.
解答 解:(1)仪器A的名称是环形玻璃搅拌棒,故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是:隔热,减少热量散失,
故答案为:隔热,减少热量散失;
(3)若保温效果不好,有热量散失,求得的中和热数值将会减小,△H大于-57.3kJ•mol-1,
故答案为:实验过程中难免有热量散失;
(4)一水合氨为弱碱,电离过程为吸热过程,用相同浓度和体积的氨水(NH3•H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小;
中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量,稀硝酸与Ba(OH)2溶液反应符合中和热的概念;
故答案为:偏小;无影响.
点评 本题考查测定反应热的误差分析,难度中等,注意理解中和热的概念.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:选择题
| A. | 加热NaHSO4至熔化NaHSO4═Na++H++SO42- | |
| B. | 把CaO放入水中CaO═Ca2++O2- | |
| C. | HClO═H++ClO- | |
| D. | H2S?H++HS-;HS-?H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CSO的电子式: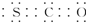 | |
| B. | Cl-的结构示意图: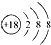 | |
| C. | 甲烷分子的比例模型: | |
| D. | 原子核内有20个中子的氯原子:2017Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
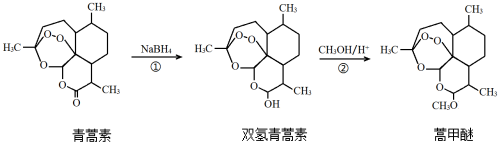
| A. | 利用黄花蒿叶研究青蒿素结构的基本步骤为:分离、提纯→元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式 | |
| B. | 双氢青蒿素在水中的溶解性大于青蒿素 | |
| C. | ①、②的反应类型分别为还原反应、取代反应 | |
| D. | 青蒿素转化为双氢青蒿素,手性碳个数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲 | B. | 乙 | C. | 丙 | D. | 丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 L 0.1 mol•L-1 (NH4)2Fe(SO4)2•6H2O溶液中:c(NH4+)+c(Fe2+)+c(H+)=c(OH-)+c(SO42-) | |
| B. | 0.1 mol•L-1的NH4Cl与0.1 mol•L-1的NH3•H2O等体积混合:c(NH4+)+2c(H+)=c(NH3•H2O)+2c(OH-) | |
| C. | pH=9.4、浓度均为0.1 mol•L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) | |
| D. | 0.1 mol•L-1 CH3COONa 溶液与0.05 mol•L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→Cu2(OH)CO3 | B. | HCl→Cl2 | C. | Fe2O3→Fe | D. | Al(OH)3→Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
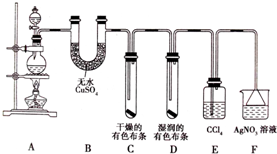 某化学实验兴趣小组为探究实验室制备Cl2 的过程中有水蒸气和HCl挥发来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略):
某化学实验兴趣小组为探究实验室制备Cl2 的过程中有水蒸气和HCl挥发来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
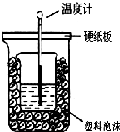 实验室利用如图装置进行中和热的测定,请回答下列问题:
实验室利用如图装置进行中和热的测定,请回答下列问题:| 反应物 | 起始温度t1/°C | 终了温度t2/°C | 中和热 |
| HCl+NaOH | 13 | 19.8 | △H1 |
| HCl+NH3•H2O | 13 | 19.3 | △H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com