
【题目】如图在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝。小心地从烧杯中央滴入硫酸铜溶液
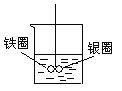
(1)片刻后可观察到的现象是(指悬吊的金属圈)(____)
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(2)铁圈是___________极,发生的电极反应:__________________
银圈是__________极,发生的电极反应:__________________。
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】甲醇燃料电池被认为是21世纪电动汽车候选动力源
(1)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2
已知H2(g)+![]() O2(g)=H2O(g) △H =-241.8 kJ·mol-1,则反应②的△H2= 。
O2(g)=H2O(g) △H =-241.8 kJ·mol-1,则反应②的△H2= 。
(2)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)![]() CH3OH(g),现实验室模拟该反应并进行分析,下图是该反应在不同温度下CO的转化率随时间变化的曲线
CH3OH(g),现实验室模拟该反应并进行分析,下图是该反应在不同温度下CO的转化率随时间变化的曲线
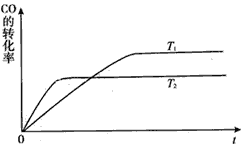
①该反应的焓变△H__________0(填“>” “<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1__________K2(填“>”“<”或“=”)
③现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO 和CH 3OH(g)的浓度随时间变化如图所示。
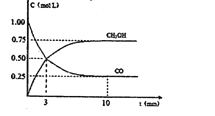
从反应开始到平衡,CO的平均反应速率v(CO)=__________,该反应的平衡常数为K=__________
④恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO )增大的有__________
A.升高温度 B.充入He(g)
C.再充入1molCO 和3molH2 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届河南省豫南九校高三下学期质量考评(五)】下列说法正确的是
A. 加热条件下才能发生的化学反应一定是吸热反应
B. 酸性溶液中水的电离程度一定比纯水的电离程度小
C. 海轮船体镶嵌锌块是牺牲阳极的阴极保护法,防止船体被腐蚀
D. 一定条件下反应2SO2+O2![]() 2SO3达到平衡时,v正(O2)=2v逆(SO3)
2SO3达到平衡时,v正(O2)=2v逆(SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在现行元素周期表中,所含元素种数最多的族和周期分别是( )
A.第ⅠA族 第6周期
B.第Ⅷ族 第6周期
C.第ⅢB族 第6周期
D.第ⅢA族 第6周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在已达到电离平衡的0.1 mol/L的醋酸溶液中,欲使平衡向电离的方向移动,同时使溶液的pH 降低,应采取的措施是
A.加热 B.加少量盐酸 C.加少量醋酸钠晶体 D.加少量水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图,下列说法正确的是( )

A. 镁作Y电极
B. 电池工作时,Na+向负极移动
C. 废液的pH大于NaClO溶液的pH
D. X电极上发生的反应为ClO-+2H2O - 4e-═ClO3-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.原电池的负极得到电子,发生还原反应
B.原电池中较活泼的金属作正极
C.原电池中的电极一定要由两种不同的金属组成
D.原电池中发生氧化反应的电极是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3CH=CHCl该有机物能发生( )
①取代反应 ②加成反应 ③消去反应 ④使溴水褪色 ⑤使酸性高锰酸钾溶液褪色 ⑥与硝酸银溶液生成白色沉淀 ⑦聚合反应
A. 以上反应均可发生 B. 只有⑦不能发生
C. 只有⑥不能发生 D. 只有②不能发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com