
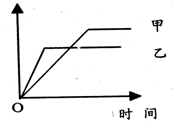
 可用下列示意图象表示的是( )
可用下列示意图象表示的是( )| 反应 | 纵坐标 | 甲 | 乙 | |
| A | 等质量的钠、钾分别与足量乙醇反应 | H2质量 | 钠 | 钾 |
| B | 在同一容器中一定质量的氨气分解 | 氨气的 转化率 |
500℃ | 400℃ |
| C | 体积比1:3的N2、H2在体积可变的恒压容器中合成氨 | 氨气的 浓度 |
活性高的催化剂 | 活性一般的催化剂 |
| D | 2molSO2与1molO2在相同温度下化合 | SO3物 质的量 |
10个 大气压 |
2个大气压 |
| A、A | B、B | C、C | D、D |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、22.4 L甲烷分子中含共价键数目为4NA |
| B、7.1 g Cl2完全反应,转移的电子数一定为0.1NA |
| C、1 mol/L的Na2CO3溶液中含有2NA个Na+ |
| D、CO2和O2组成的混合物中含有NA个分子,其中氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、Na+、SO42-、SCN- |
| B、Na+、Ca2+、HCO3-、OH- |
| C、Na+、H+、ClO-、S2- |
| D、NH4+、Fe2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打与盐酸反应:CO32-+2H+═CO2↑+H2O |
| B、碳酸钠水解:CO32-+H2O?HCO3-+OH- |
| C、用食醋除去水垢:CaCO3+2H+═CO2↑+H2O+Ca2+ |
| D、硫酸溶液与氢氧化钡溶液反应:OH-+H+═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A、d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
| B、b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3- |
| C、c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ |
| D、a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含12.0 g NaHSO4晶体中阳离子数约为0.2×6.02×1023 |
| B、在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
| C、常温常压下,氧气和臭氧的混合物16g中约含有6.02×1023个氧原子 |
| D、一定温度下,1 L 0.50 mol?L-1NH4Cl与2 L 0.25 mol?L-1 NH4Cl两种溶液含n(NH+4)不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeBr2溶液中加入过量的氯水:2Fe2++2Br-+2Cl2═Br2+4Cl-+2Fe3+ |
| B、向小苏打溶液中加入醋酸:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- |
| C、向碳酸氢铵溶液中加入少量氢氧化钠:HCO3-+OH-═CO32-+H2O |
| D、用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O═2HCO3-+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
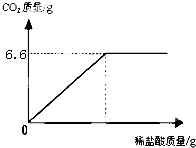 某同学从制碱厂带回一瓶废弃的纯碱样品,决定测定其中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质).她取样品30g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示,
某同学从制碱厂带回一瓶废弃的纯碱样品,决定测定其中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质).她取样品30g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com