
| A、硫离子的核外电子排布式:1s22s22p63s23p6 |
| B、N2的结构式::N≡N: |
C、NaCl的电子式: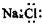 |
D、CO2的分子模型示意图: |
 ,故C错误;
,故C错误;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,将甲酸钠和适量盐酸混合,若所得的溶液恰好呈中性,则粒子间存在大小关系:c(Na+)>c(HCOO-)>c(HCOOH)>c(H+)=c(OH-) |
| B、将amol/L的Na2RO3溶液与bmol/L的NaHRO3溶液等体积混合,若离子间存在大小关系:c(Na+)>c(HRO3-)>c(RO32-)>c(OH-)>c(H+),则有:a<b |
| C、若KHA溶液呈酸性,则离子间一定存在大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) |
| D、向硝酸银溶液中逐滴滴加物质的量浓度相等的氯化钾和铬酸钾的混合溶液,若先产生白色的氯化银沉淀,则有:Ksp(AgCl)<Ksp(Ag2CrO4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应过程中,当A、B、C的物质的量浓度之比为2:1:2时,反应即达到平衡状态 |
| B、达平衡后若升高温度,C的浓度将增大 |
| C、达平衡后若增大压强,A的转化率降低 |
| D、4 s内用物质B表示的反应速率为0.075 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用盐酸与苛性钠的反应,可以制成原电池,将化学能转化为电能 |
| B、化学反应中的能量变化的大小与反应物的质量多少无关 |
| C、化学变化中的能量变化主要是由化学键变化引起的 |
| D、燃料电池的能量转化率可达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化合价高低 |
| B、氢化物的稳定性 |
| C、元素在周期表中的位置 |
| D、最高价氧化物对应水化物的酸性或碱性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2+CuO
| ||||
| B、2Na2O2+2H2O═4NaOH+O2↑ | ||||
C、2KClO3
| ||||
| D、2NaOH+Cl2═NaCl+NaClO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A是固体,C是气体,正反应吸热 |
| B、A是气体,C是固体或液体,正反应放热 |
| C、A是气体,C是气体,正反应放热 |
| D、A是气体,C是气体,正反应吸热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com