
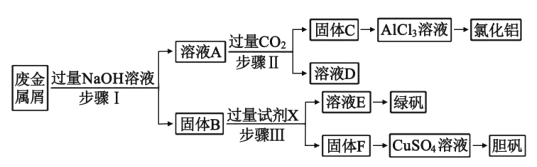
【题目】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
请回答:
(1)步骤Ⅰ中,发生的氧化还原反应的离子方程式为___,涉及到的分离操作是___。
(2)试剂X是___;溶液D是___。
(3)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化___。
(4)在步骤Ⅱ时,若用大理石与浓盐酸制取CO2并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是___。
(5)工业上常用溶液E制取净水剂Na2FeO4,流程如图:
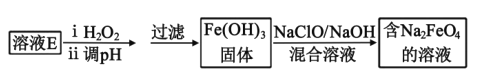
写出由Fe(OH)3制取Na2FeO4的离子方程式___。(已知NaClO还原为NaCl)
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑ 过滤 稀硫酸(或稀H2SO4;或硫酸) NaHCO3溶液(或碳酸氢钠溶液) 取少量E溶液于试管中,滴入几滴硫氰化钾溶液,若溶液变为血红色,则说明E溶液已被氧化,反之,则未被氧化 在通入CO2之前增加一个盛有饱和NaHCO3溶液的洗气瓶,除去HCl气体 2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
【解析】
Cu、Fe和Al,少量Al2O3和Fe2O3,氢氧化钠与Al、Al2O3反应,而Cu、Fe和Fe2O3不反应,过滤得到滤渣为Cu、Fe和Fe2O3,滤液为偏铝酸钠溶液和氢氧化钠溶液,向滤液中通入过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠溶液,过滤,向沉淀中加入盐酸生成氯化铝溶液,最终得到氯化铝固体;向滤渣为Cu、Fe和Fe2O3中加入稀硫酸,生成硫酸亚铁,最终得到绿矾,过滤得到Cu,Cu与氧气、硫酸反应得到硫酸铜。
⑴步骤Ⅰ中,发生的氧化还原反应的是铝和氢氧化钠反应生成偏铝酸钠和氢气,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,Fe、Cu、Fe2O3不和氢氧化钠溶液反应,因此涉及到的分离操作是过滤;故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;过滤。
⑵将Fe、Cu中Fe溶于溶液中生成硫酸亚铁,因此试剂X是硫酸;溶液A为偏铝酸钠溶液,向溶液中通入过量二氧化碳,反应生成氢氧化铝沉淀和碳酸氢钠溶液,因此D是碳酸氢钠;故答案为:稀硫酸(或稀H2SO4;或硫酸);NaHCO3溶液(或碳酸氢钠溶液)。
⑶溶液E在空气中易被氧化,亚铁离子被氧化生成铁离子,铁离子常用KSCN溶液来检验,因此简单的实验方案检验溶液E是否被氧化的实验为取少量E溶液于试管中,滴入几滴硫氰化钾溶液,若溶液变为血红色,则说明E溶液已被氧化,反之,则未被氧化;故答案为:取少量E溶液于试管中,滴入几滴硫氰化钾溶液,若溶液变为血红色,则说明E溶液已被氧化,反之,则未被氧化。
⑷在步骤Ⅱ时,若用大理石与浓盐酸制取CO2并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少,减少的主要原因是浓盐酸易挥发,挥发出的HCl与沉淀反应,为避免固体C减少,先用饱和碳酸氢钠溶液除掉挥发的HCl,再通入CO2;故答案为:在通入CO2之前增加一个盛有饱和NaHCO3溶液的洗气瓶,除去HCl气体;故答案为:在通入CO2之前增加一个盛有饱和NaHCO3溶液的洗气瓶,除去HCl气体。
⑸Fe(OH)3与NaClO反应生成NaCl和Na2FeO4,其制取Na2FeO4的离子方程式2Fe(OH)3+3ClO-+4OH- = 2FeO42+3Cl-+5H2O;故答案为:2Fe(OH)3+3ClO-+4OH- = 2FeO42+3Cl-+5H2O。


科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴入某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:![]() ]。下列叙述不正确的是
]。下列叙述不正确的是

A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液的过程中,![]() 保持不变
保持不变
C. m点所示溶液中:c(H+)+c(Na+)=c(HA)+c(OH-)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究一溴环己烷(![]() )与NaOH 的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计了如下三种实验方案。
)与NaOH 的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计了如下三种实验方案。
甲:向反应混合液中滴入稀硝酸中和NaOH 溶液,然后滴入AgNO3溶液,若有淡黄色沉淀生成,则可证明发生了消去反应。
乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。
丙:向反应混合液中滴入酸性FeCl3溶液,若溶液颜色变为紫色,则可证明发生了水解反应。
其中正确的是( )
A.甲B.乙
C.丙D.上述实验方案都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由SiO2、Fe2O3、Fe、Na2SO3、Na2CO3、BaCl2中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计的部分实验方案如下图所示:

下列说法正确的是( )
A. 气体A是SO2和CO2的混合气体
B. 固体A一定含有SiO2,可能含有BaSO4
C. 该固体混合物中Fe2O3和Fe至少有其中一种
D. 该固体混合物一定含有Fe、Na2SO3、BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种有机物的转化关系如下图所示(部分条件已省略)
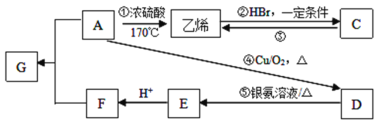
(1)反应①的化学方程式为____________________,反应类型为_________。
(2)③的试剂及反应条件是____________。
(3)写出反应④的化学方程式___________________。
(4)写出反应⑤的化学方程式__________________。
(5)写出A+F反应生成G的化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移电子总数为0.1mol
B.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,所以明矾可用于水的净化
C.向Na2CO3溶液中滴加盐酸溶液,一定有CO2气体生成
D.Na2O2常用于潜水艇或呼吸面具的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中的微粒浓度关系不正确的是
A. pH=8.3的某酸式盐NaHB的水溶液中:c (Na+) > c (HB-) > c (H2B) > c (B2-)
B. 等物质的量浓度的Na2S和NaHS溶液中:c (Na+)=2c (S2-) + c (HS-)
C. NH4HSO4溶液中滴加NaOH溶液至恰好呈中性:c (Na+) > c (SO42-) > c (NH4+) > c (OH-)=c (H+)
D. 0.1 mol / L NaH2PO4溶液中:c (Na+)=c (PO43-) + c (HPO42-) + c (H2PO4-) + c (H3PO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究乙醇和金属钠反应生成![]() 的原理,某同学做了如下四个实验。
的原理,某同学做了如下四个实验。
甲:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体
乙:设法检验甲收集到的气体。
丙:向试管中加人![]() 水,并加入绿豆粒大小的金属钠,观察现象。
水,并加入绿豆粒大小的金属钠,观察现象。
丁:向试管中加人![]() 乙醚(
乙醚(![]() ),并加入绿豆粒大小的金属钠,发现无明显变化。
),并加入绿豆粒大小的金属钠,发现无明显变化。
回答以下问题:
(1)从结构上分析,该实验选取水和乙醚作参照物的原因是__________。
(2)丙的目的是证明_____________;丁的目的是证明_______;根据丙和丁的结果,可以得出乙醇和金属钠反应的化学方程式应为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是

A. B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C点水电离的c(OH-)大于A点水电离的c(OH-)
D. A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com