
| | 水 | 四氯化碳 |
| 溴 | 黄→棕 | 橙→橙红 |
| 碘 | 深黄→褐 | 紫→深紫 |
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| A.X2YZ4 | B.X2YZ3 | C.X3YZ4 | D.XY2Z3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 离子化合物 | AB | CD | EF |
| 离子电荷数 | 1 | 1 | 2 |
| 键长(10-10m) | 2.31 | 3. 18 | 2.10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 I健康相关知识答问”中指出,
I健康相关知识答问”中指出, I是人工放射性核素,正常情况下自然界中不会存在,日本核泄漏事故释放的放射性核素中含有这种核素。下列有关
I是人工放射性核素,正常情况下自然界中不会存在,日本核泄漏事故释放的放射性核素中含有这种核素。下列有关 I的叙述正确的是
I的叙述正确的是| A.是碘的一种同素异形体 | B.是一种新发现的元素 |
| C.核内的中子数与核外电子数之差为25 | D.位于元素周期表中第4周期ⅦA族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.131I、132I、134Cs、137Cs是四种不同的核素 | B.食用碘盐不能防辐射 |
| C.碘片的主要成分是I2 | D.核能仍然是重要能源之一 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 结构或性质信息 |
| M | M的一种单质是自然界最硬的物质 |
| Q | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
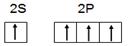 ,请判断对错,并加以解释
,请判断对错,并加以解释  电子式___________
电子式___________ 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
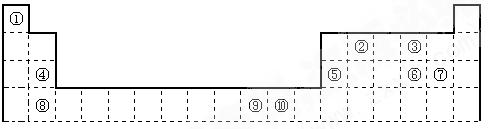
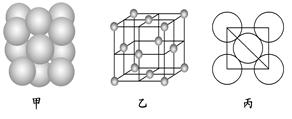
 晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。
晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。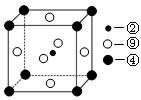
 油化工发展水平的标志。有关该氢化物分子的说法正确的是
油化工发展水平的标志。有关该氢化物分子的说法正确的是  。
。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
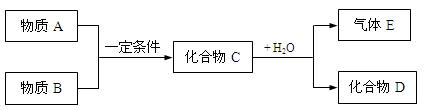
 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com