
某校化学小组学生进行“气体相对分子质量的测定”的实验.操作如下:用质量和容积都相等的烧瓶收集气体,称量收集满气体的烧瓶质量.数据见下表(已换算成标准状况下的数值).
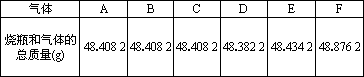
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.421 2 g.空气的平均相对分子质量为29.A、B、C、D、E、F是中学常见的气体.
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)________.
(2)E的相对分子质量是________.
(3)实验室制取少量D的化学方程式是________.
(4)A、B、C可能的化学式是________.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 气体 | A | B | C | D | E | F |
| 烧瓶和 气体的 总质量(g) |
48.408 2 | 48.408 2 | 48.408 2 | 48.382 2 | 48.434 2 | 48.876 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
气体 | A | B | C | D | E | F |
烧瓶和气体的总质量/g | 48.4082 | 48.4082 | 48.4082 | 48.3822 | 48.4342 | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.4212 g。空气的平均相对分子质量为29。A、B、C、D、E、F是中学常见的气体。
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)________________。
(2)E的相对分子质量是________。
(3)实验室制取少量D的化学方程式是______________________________。
(4)A、B、C可能的化学式是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
气体 | A | B | C | D | E | F |
烧瓶和气体的总质量/g | 48.4082 | 48.4082 | 48.4082 | 48.3822 | 48.4342 | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.4212 g。空气的平均相对分子质量为29。A、B、C、D、E、F是中学常见的气体。
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)________________。
(2)E的相对分子质量是_________。
(3)实验室制取少量D的化学方程式是________________________________________。
(4)A、B、C可能的化学式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学小组学生进行“气体相对分子质量的测定”的实验。操作如下:用质量和容积都相等的烧瓶收集气体,称量收集满气体的烧瓶质量。数据见下表(已换算成标准状况下的数值)。?
气体 | A | B | C | D | E | F |
烧瓶和气体的总质量/g | 48.4082 | 48.408 2 | 48.4082 | 48.3822 | 48.4342 | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.4212 g。空气的平均相对分子质量为29。A、B、C、D、E、F是中学常见的气体。?
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)_______________。
(2)E的相对分子质量是____________。
(3)实验室制取少量D的化学方程式是____________________________________。
(4)A、B、C可能的化学式是__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)使用铜和稀硫酸制备硫酸铜晶体?
步骤如下:?
![]()
步骤①观察到的现象是 。?
步骤③的主要操作包括: 。
(2)某硫酸铜晶体(CuSO4·nH2O)中含有少量的氯化钠,实验室里测定结晶水n的数值?
A.在实验过程中要用到下列仪器中的 (填序号,下同)。?
①容量瓶 ②托盘天平 ③烧杯 ④锥形瓶 ?⑤漏斗? ⑥干燥器 ⑦长颈漏斗 ⑧试管 ⑨试管夹 ?⑩坩埚?
B.在下列操作中,选用必要的步骤,按操作先后顺序排列 。?
①称量硫酸铜晶体 ②加水溶解 ③过滤 ④加过量AgNO3溶液 ⑤称出加热后固体质量 ⑥加热⑦加过量BaCl2溶液 ⑧称量沉淀?
C.在以上操作中,若硫酸铜晶体质量为a g,沉淀质量为b g,加热后固体质量为c g,则a g硫酸铜晶体中结晶水n为 。?
(3)硫酸铜溶解度的测定?
用石墨电极(相同)电解饱和CuSO4溶液,阴极的电极反应式是 。
已知饱和CuSO4溶液的质量为60 g,通电10 min后,溶液恰好变为无色。称量发现两电极质量差为4 g,此温度下CuSO4的溶解度是 。?
(4)已知铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解。请写出该反应的化学方程式: 。?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com