
【题目】中国科学家用蘸墨汁书写后的纸张作空气电极(图1),设计并组装出一种轻型、能折叠的可充电锂空气电池,其工作原理如图2所示。下列有关说法正确的是

A.闭合开关K给锂电池充电,X为直流电源负极
B.放电时,纸张中的纤维素作锂电池的正极
C.放电时,Li+由正极经过液相有机电解质移向负极
D.充电时,阳极的电极反应式为Li2O2+2e -=O2↑+2Li+
科目:高中化学 来源: 题型:
【题目】如图是一种可充电锂电池,反应原理是4Li+FeS2![]() Fe+2Li2S,LiPF6是电解质,SO(CH3)2是溶剂。下列说法正确的是( )
Fe+2Li2S,LiPF6是电解质,SO(CH3)2是溶剂。下列说法正确的是( )
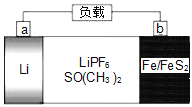
A.放电时,电子由a极经电解液流向b极
B.放电时,电解质溶液中PF6-向b极区迁移
C.充电时,b极反应式为Fe+2Li2S-4e-=FeS2+4Li+
D.充电时,b极消耗5.6gFe时在a极生成0.7gLi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向一个2 L的真空密闭容器中(预先装入催化剂)通入1 mol N2和3 mol H2,经过一段时间后,测得容器内压强是起始时的0.9倍。在此时间段内H2的平均反应速率为0.1 mol·L-1·min-1,则经过时间为( )
A. 2 minB. 3 minC. 4 minD. 5 min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原儿茶醛是一种医药中间体,一种合成路线如图: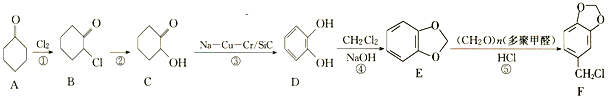
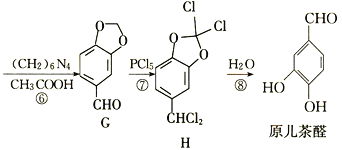
回答下列问题:
(1)A中的官能团名称是________。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。B中____(填“有”或“没有”)手性碳。
(3)反应①的类型是__________;反应②所需试剂和条件分别为________。
(4)原儿茶醛的分子式为________。
(5)W与C互为同分异构体,W中不含环状结构,能发生水解反应,核磁共振氢谱只有3组峰且峰面积之比为6∶3∶1,W的结构简式为_________(只写一种)。
(6)设计以苯酚和(CH2O)n为原料制备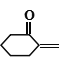 的合成路线_______。(无机试剂任选)。已知:苯酚在多聚甲醛和氯化氢作用下,在邻位发生取代反应。
的合成路线_______。(无机试剂任选)。已知:苯酚在多聚甲醛和氯化氢作用下,在邻位发生取代反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上苯乙烯是合成树脂、离子交换树脂及合成橡胶等的重要单体,如图是苯乙烯的结构简式:![]() ,下列关于该有机物的说法不正确的是( )
,下列关于该有机物的说法不正确的是( )
A. 苯乙烯的分子式为C8H8
B. 苯乙烯通过加聚反应可制备高分子化合物
C. 苯乙烯与溴的四氯化碳溶液反应:![]()
D. 苯乙烯能发生加成反应,但不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物H是一种光刻胶,其中的一种合成路线如下:

回答下列问题:
(1)B的化学名称是_________。
(2)B生成C的反应类型为_________,F与G反应生成H的反应类型为_________。
(3)H中官能团的名称为___________________________。
(4)C的结构简式为__________________,G的结构简式为__________________。
(5)已知E与D,F与CH3OH分别含有相同的官能团,写出D与CH3OH反应生成E和F的化学方程式:________。
(6)芳香族化合物X是G的同分异构体,1 mol X与足量银氨溶液反应生成4 mol Ag,则X的结构简式有_____(不考虑立体异构)种,写出核磁共振氢谱显示有五种不同化学环境的氢,且峰面积之比为1:2:2:2:1的X的结构简式:___________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
|
|
|
|
NaCl溶于水 | 铁的吸氧腐蚀原理 | 铜锌原电池构造和原理 | N2与O2反应能量变化 |
NaCl=Na+ + Cl- | 负极:Fe - 2e-=Fe2+ | 总反应:Zn + Cu2+=Zn2+ + Cu | N2(g) + O2(g)=2NO(g)ΔH=-180 kJ·mol-1 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某烧碱样品的纯度,请回答下列问题:
(1)准确称量5.0 g含有少量易溶杂质的样品(杂质不与盐酸反应),配成250 mL待测溶液,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、___________________。
(2)滴定时,用0.2000 mol·L-1的盐酸来滴定待测溶液,量取待测液10.00 mL应选用_________仪器(填字母)。

(3)滴定过程中,眼睛应注视___________________________________,以甲基橙做指示剂,正确判断滴定终点的现象是________________________________。
(4)由下表可知,第2次所用盐酸体积明显偏大,其可能的原因是_________。
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 2.10 | 24.20 |
第三次 | 10.00 | 4.10 | 24.00 |
a.锥形瓶用待测液润洗
b.滴定过程中锥形瓶中溶液溅出瓶外
c.滴定前滴定管尖嘴有气泡,滴定结束气泡消失
d.滴定结束时,俯视读数
(5)根据表中数据,计算被测烧碱溶液的物质的量浓度是_________,烧碱样品的纯度是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com