
已知A、B、C、D、E、F都是元素周期表前四周期的元素,它们的核电荷数:B<A<C<D<E<F。B、C两种元素都能引起水体富营养化。E原子得到一个电子后3p轨道全充满。A+比E原子形成的离子少1个电子层。D可以形成两种氧化物,其中一种氧化物是形成酸雨的主要气体之一。F的原子序数为26。请回答下列问题:
(1)C、D、E的第一电离能由小到大的顺序为________(用元素符号表示)。
(2)写出B的氢化物与水反应的离子方程式:________________,B的氢化物
极易溶于水的原因是________________________________________________
_________________________________________________________________。
(3)化合物BE3的分子空间构型为________________。
(4)F元素原子的核外电子排布式为________。F的一种常见化合物F(CO)5在
常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,则F(CO)5
的晶体类型为__________________。
(5)将FE3的饱和溶液滴入沸水中,请写出有关反应的离子方程式:_________
_________________________________________________________________。
(6)比较B、C两种元素的氢化物稳定性并说明理由: ____________________。
解析 能引起水体富营养化的元素为N、P,由题意可知B为氮元素,C为
磷元素。同时可以确定A为钠元素,E为氯元素。由“D可以形成两种氧化
物,其中一种氧化物是形成酸雨的主要气体之一”可推出D为硫元素。由“F
的原子序数为26”可知F为铁元素。
答案 (1)S<P<Cl
(2)NH3+H2ONH3·H2ONH4++OH- NH3与H2O之间能形成氢
键;NH3和H2O都是极性分子,根据“相似相溶”原理,NH3在H2O中的溶
解度较大
(3)三角锥形
(4)1s22s22p63s23p63d64s2或[Ar]3d64s2 分子晶体
(5)Fe3++3H2O Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
(6)稳定性:NH3>PH3,键长越短,键能越大,化合物越稳


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
有机物M的结构简式如图所示。
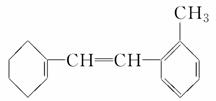
(1)有机物M的苯环上的一氯代物有________种。
(2)1 mol M与足量溴水混合,消耗Br2的物质的量为________mol。
(3)1 mol M与足量H2加成,消耗H2________ mol。
(4)下列有关M的说法中不正确的是________。
A.在催化剂的作用下,M可与液溴发生取代反应
B.M使溴水褪色的原理与乙烯使溴水褪色的原理相同
C.M能使酸性KMnO4溶液褪色
D.M和甲苯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
有①H2NCH2COOH ②CH2OH(CHOH)4CHO
③(C6H10O5)n(纤维素) ④HCOOC2H5 ⑤苯酚 ⑥HCHO等物质,其中(用数字序号填空):
(1)难溶于水的是________,易溶于水的是________,常温下微溶于水的是________。
(2)能发生银镜反应的是________。
(3)能发生酯化反应的是________。
(4)能跟氢气发生加成反应的是________,能在一定条件下跟水反应的是________。
(5)能跟盐酸反应的是________,能跟氢氧化钠溶液反应的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
充分燃烧某糖,消耗的O2、生成的CO2和H2O的物质的量都相等,它的相对分子质量是它最简式式量的6倍,0.1 mol 该糖能还原银氨溶液生成21.6 g银,0.1 mol该糖能与30 g乙酸发生酯化反应。求该糖的:
(1)最简式。
(2)相对分子质量、分子式。
(3)若该糖是直链分子,已知同一个碳原子上连有2个—OH不稳定,试推导其结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化碳晶体是新发现的高硬度材料,该晶体类型应该是________晶体。试根据物质结构推测,氮化碳晶体与金刚石相比较,硬度更大的应该是________晶体,熔点较低的应是________晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
A.花生油是纯净物,油脂是油和脂肪的总称
B.不含杂质的油脂是纯净物
C.动物脂肪和矿物油都属于油脂
D.同种单甘油酯可组成纯净物,同种混甘油酯也可组成纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)从油脂A的结构简式
 分析,它可能发生的化学反应;
分析,它可能发生的化学反应;
①从饱和性看,它能发生________反应,例如与氢气反应的化学方程式为
________________________________________________________________。
②从酯的性质看,它能发生________反应,该反应的化学方程式为
________________________________________________________________。
(2)列举硬化油的性质和用途____________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由锌、 铁、 铝、 镁四种金属中的两种组成的混合物10 g与足量的盐酸反应产生的氢气在标准状况下为11.2 L, 则混合物中一定含有的金属是 ( )
A.锌 B.铁 C.铝 D.镁
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备直径为1~100 nm的颗粒Y(化合物),反应原理为:
3Fe2+ + 2S2O32- + O2 + aOH-== Y+ S4O62- + 2H2O,下列说法中不正确的是
A.a=4
B.将Y均匀分散到水中形成的体系具有丁达尔效应
C.每有3 mol Fe2+ 参加反应,反应中转移的电子总数为5 mol
D.S2O32-是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com