
分析 (1)根据n=cV计算NaOH的物质的量,再根据m=nM计算NaOH的质量;
(2)根据n=cV计算NaOH的物质的量,根据方程式计算消耗H2SO4的物质的量,根据V=$\frac{n}{c}$计算需要硫酸溶液体积.
解答 解:(1)n(NaOH)=0.5L×0.1mol/L=0.05mol,则m(NaOH)=0.05mol×40g/mol=2.0g,
答:需要NaOH固体质量为2.0g;
(2)100mL溶液中NaOH物质的量为0.1L×0.1mol/L=0.01mol,
由2NaOH+H2SO4=Na2SO4+H2O,可知需要H2SO4 的物质的量为0.01mol×$\frac{1}{2}$=0.005mol,故所需H2SO4溶液的体积为$\frac{0.005mol}{0.1mol/L}$=0.05L,即所需H2SO4溶液的体积为50mL,
答:所需H2SO4溶液的体积为50mL.
点评 本题考查物质的量浓度有关计算,注意对物质的量浓度定义式的理解与灵活运用,有利于基础知识的巩固.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
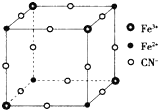 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )| A. | 该晶体的化学式为MFe2(CN)6 | |
| B. | 该晶体熔融可导电,且属于化学变化 | |
| C. | 该晶体属于离子晶体,M呈+2价 | |
| D. | 晶体中与每个Fe3+距离最近且等距离的CN-为6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ③⑤ | D. | ④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物的光合作用使得太阳能转化为了化学能 | |
| B. | 燃料燃烧时只是将化学能转化为了热能 | |
| C. | 生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理、有效 | |
| D. | 人类使用照明设备是将电能转化为了光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 15N与14N互为同位素 | ||
| C. | 13C与C60互为同素异形体 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑧ | B. | ②⑥⑧ | C. | ①③④⑦⑧ | D. | ①③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com