
【题目】尼泊金正丁酯![]() 是一种高效低毒的防腐剂
是一种高效低毒的防腐剂![]() 某研究小组采用的合成路线如下:
某研究小组采用的合成路线如下:
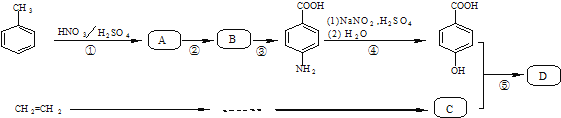
已知:
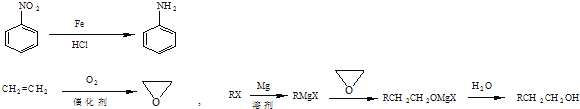
请回答下列问题:
![]() 化合物B的名称是 ______ ,其中的官能团有 ______ .
化合物B的名称是 ______ ,其中的官能团有 ______ .
![]() 第
第![]() 步属于 ______ 反应
步属于 ______ 反应![]() 填反应类型
填反应类型![]() .
.
![]() 两步的反应次序不能颠倒,其理由是 ______ .
两步的反应次序不能颠倒,其理由是 ______ .
![]() 请写出同时符合下列条件的A的同分异构体的结构简式 ______
请写出同时符合下列条件的A的同分异构体的结构简式 ______ ![]() 任写3种
任写3种![]() .
.
![]() 分子结构中有醛基
分子结构中有醛基
![]() 谱显示有苯环,且苯环上只有两种氢原子
谱显示有苯环,且苯环上只有两种氢原子
![]() 写出第
写出第![]() 步反应的化学方程式 ______ .
步反应的化学方程式 ______ .
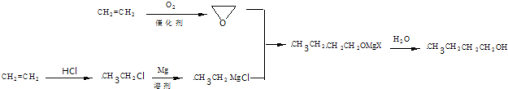
![]() 请以乙烯为原料,结合题中所给信息,设计化合物C的合成路线
请以乙烯为原料,结合题中所给信息,设计化合物C的合成路线![]() 无机试剂及溶剂任选
无机试剂及溶剂任选![]() 合成路线的书写格式参照如下示例流程图:
合成路线的书写格式参照如下示例流程图: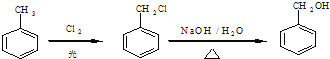 _______________
_______________
【答案】对硝基苯甲酸 硝基、羧基 氧化 如果第![]() 步进行还原反应,则在第
步进行还原反应,则在第![]() 步氨基会被氧化
步氨基会被氧化 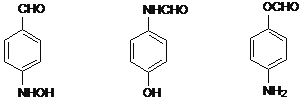

【解析】
根据题中各物质的转化关系,根据![]() 的结构可知,甲苯发生硝化反应生成A为
的结构可知,甲苯发生硝化反应生成A为![]() ,A发生氧化反应生成B为
,A发生氧化反应生成B为![]() ,B发生还原反应得
,B发生还原反应得![]() ,根据D的分子式和
,根据D的分子式和![]() 的结构可知,C为
的结构可知,C为![]() ,乙烯被氧气氧化成
,乙烯被氧气氧化成![]() ,同时乙烯与氯化氢加成得
,同时乙烯与氯化氢加成得![]() ,
,![]() 发生信息中的反应生成
发生信息中的反应生成![]() ,
,![]() 与
与![]() 反应生成
反应生成![]() ,
,![]() 水解得
水解得![]() ,据此答题。
,据此答题。
根据题中各物质的转化关系,根据![]() 的结构可知,甲苯发生硝化反应生成A为
的结构可知,甲苯发生硝化反应生成A为![]() ,A发生氧化反应生成B为
,A发生氧化反应生成B为![]() ,B发生还原反应得
,B发生还原反应得![]() ,根据D的分子式和
,根据D的分子式和![]() 的结构可知,C为
的结构可知,C为![]() ;
;
![]() 根据上面的分析可知,B为
根据上面的分析可知,B为![]() ,B的名称是对硝基苯甲酸,其中的官能团有硝基、羧基;
,B的名称是对硝基苯甲酸,其中的官能团有硝基、羧基;
![]() 第
第![]() 步属于氧化反应;
步属于氧化反应;
![]() 两步的反应次序不能颠倒,因为如果第
两步的反应次序不能颠倒,因为如果第![]() 步进行还原反应,则在第
步进行还原反应,则在第![]() 步氨基会被氧化;
步氨基会被氧化;
![]() 的同分异构体符合下列条件
的同分异构体符合下列条件![]() 分子结构中有醛基;
分子结构中有醛基;![]() 谱显示有苯环,且苯环上只有两种氢原子,符合条件的结构简式为
谱显示有苯环,且苯环上只有两种氢原子,符合条件的结构简式为 ;
;
![]() 第
第![]() 步反应的化学方程式为
步反应的化学方程式为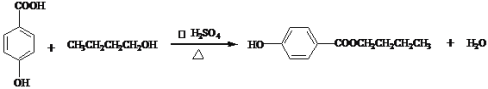 ;
;
![]() 以乙烯为原料,合成
以乙烯为原料,合成![]() ,可以将乙烯与氧气氧化成
,可以将乙烯与氧气氧化成![]() ,同时乙烯与氯化氢加成得
,同时乙烯与氯化氢加成得![]() ,
,![]() 发生信息中的反应生成
发生信息中的反应生成![]() ,
,![]() 与
与![]() 反应生成
反应生成![]() ,
,![]() 水解得
水解得![]() ,合成路线为
,合成路线为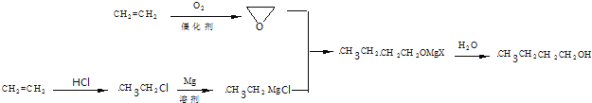 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目。____________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______,MnO![]() +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)6.02×1023个氢氧根离子的物质的量是________mol,其摩尔质量为________。
(2)3.01×1023个H2O的物质的量为________mol,其中,所有原子的物质的量为________mol,所含电子的物质的量为________mol。
(3)1.204×1023个![]() 的物质的量为________mol,质量为________g。
的物质的量为________mol,质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
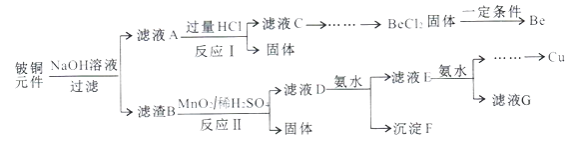
已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下:Ksp[Cu(OH)2]=2.2×10-20, Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13。
回答下列问题:
(1)滤液A的主要成分除NaOH外,还有___________(填化学式);写出反应I中含铍化合物与过量盐酸反应的离子方程式:___________。
(2)滤液C中含NaCl、BeCl2和少量HCl,为得到较纯净的BeCl2溶液,选择下列实验操作最合理步骤的顺序是___________;电解熔融BeCl2制备金属铍时,需要加入NaCl,其作用是___________。
①加入过量的NaOH:②加入过量的氨水;③加入适量的HCl;④过滤;⑤洗涤。
(3)反应Ⅱ中CuS的氧化产物为S单质,该反应的化学方程式为___________。
(4)常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是________(填化学式);为了尽可能多的回收铜,所得滤液G的pH最大值为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐渐加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的下列说法中,不正确的是( )
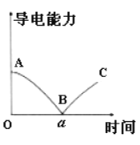
A.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质
B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
C.BC段溶液的导电能力不断增大,主要是由于过量的H2SO4电离出的离子导电
D.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取、净化并收集氯气涉及以下几个主要阶段:![]()
![]()
![]()
![]() 尾气处理
尾气处理
(1)写出实验室制取Cl2的离子方程式______________________,NA表示阿伏加德罗常数,若有4mol的HCl参加反应,则转移的电子总数为___________;
(2)现有以下3种试剂:A.饱和食盐水 B.浓硫酸 C.NaOH溶液
请在以上试剂中选择并回答填空:
X溶液应选用_________(填写序号);Y试剂的作用____________________.
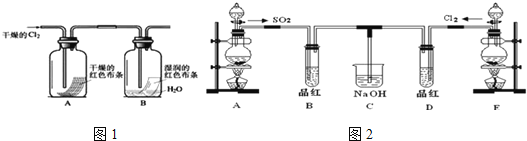
(3)某化学兴趣小组为了探究Cl2的相关性质,设计了如图1的实验.
通入Cl2后,从观察集气瓶A、B中的现象可得出的结论是_____________(写出化学反应方程式,并用简要文字解释).
(4)某兴趣小组的同学为探究和比较SO2和氯水的漂白性,设计了如图2的实验装置.
①实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:______________________;
②反应开始一段时间后,观察到B、D两试管中的品红溶液都出现褪色的现象,但两者褪色原理不同,如何区别,请你帮助设计实验,你的操作是_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液的性质与变化是多样的,下列说法正确的是( )
A. pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③
B. 往稀氨水中加水,![]() 的值变小
的值变小
C. pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+)c=(OH—)+2c(S2—)
D. Ca(ClO)2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学教师为“氯气与金属钠反应”设计了如图装置的实验。实验操作:先给钠预热,等钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述中错误的是( )

A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气
C. 钠着火燃烧产生苍白色火焰
D. 若在棉花球外沿滴一滴石蕊溶液,可根据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com