
【题目】常温下,稀释0.5mol·L-1的醋酸溶液,下图中的纵坐标不能表示
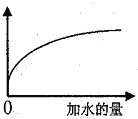
A. CH3COOH的电离程度 B. 溶液中H+的数目
C. 溶液中OH-的浓度 D. 溶液中CH3COOH的浓度
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将Na2O2分别投入下列物质的水溶液中,生成白色沉淀的是( )
A. BaCl2 B. K2SO4 C. CuCl2 D. Ca(HCO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值,下列叙述不正确的是
A. 常温常压下,1.7 g氨气中含有的原子数目为0.4NA
B. 50 mL 1 mol·L1 K2SO4溶液中含有的K+数目为0.1NA
C. 5.6 g铁与足量稀硫酸反应转移的电子数为0.3NA
D. 标准状况下,4.48 L的氧气和氮气的混合物含有的分子数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是 ( )

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G[ ]是一种医药中间体,它的一种合成路线如下:
]是一种医药中间体,它的一种合成路线如下:

已知:
请回答下列问题:
(1)A的名称是_____________。
(2)B→C的反应条件为_____________。
A→B和D→E的反应类型分别是_____________、_____________。
(3)D在浓硫酸加热的条件下会生成一种含六元环的化合物,该化合物的结构简式为_____________。(4)H是一种高聚酯,D→H的化学方程式为_____________。
(5)下列关于化合物G的说法错误的是_____________。
A.G的分子式为C12H14O5
B.1molG与NaOH溶液加热最多消耗2molNaOH
C.一定条件下G发生消去反应生成的有机物存在顺反异构体
D.在一定条件下G能与HBr发生取代反应
(6)M是D的同分异构体,与D具有相同的官能团。则M可能的结构有____种。
(7)已知酚羟基不易与羧酸发生酯化反应,写出由苯酚,甲苯为原料制备苯甲酸苯酚酯(![]() )的合成路线(其它试剂任选)。 __________________
)的合成路线(其它试剂任选)。 __________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.2molMn02和50mL12mol/L盐酸混合后加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发)( )
A. 等于0.3mol B. 小于0.3mol C. 大于 0.3mol,小于 0.6mol D. 等于 0.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设在容积可变的密闭容器中充入10 mol N2(g)和10 mol H2(g),反应在一定条件下达到平衡时,NH3的体积分数为0.25。计算[(1)、(2)的计算都需按格式写计算过程,否则答案对也不给分]
(1)该条件下反应N2(g)+3H2(g)![]() 2NH3(g) 的平衡常数________。(设该条件下,每1mol气体所占的体积为VL)
2NH3(g) 的平衡常数________。(设该条件下,每1mol气体所占的体积为VL)
(2)上述反应的平衡时,再充入10 mol的N2,根据计算,平衡应向什么方向移动________
(3)某温度下将所得的氨气配成0.1 molL-1的溶液,所得溶液的pOH_____;将该溶液冲稀100倍;计算此时氨水的电离度为________(已知该温度下Kb(NH3·H2O) =1.0×10-5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铝的熔点很高,常用于制造耐火材料,例如制作坩埚。下列操作不能在氧化铝坩埚中进行的是
A.加热使胆矾失去结晶水B.加热使高锰酸钾分解
C.加热熔化烧碱D.加热分解碱式碳酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的转化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是______。
(2)根据上图反应关系,写出下列B、F所含物质成分的化学式:B______;F_____。
(3)写出过程反应①的离子方程式_________________,固体B所含对应的金属其单质与磁性氧化铁在高温下反应的化学方程式__________________________。
(4)写出③中盐酸过量时的离子反应方程式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com