
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e-
D.铝热法还原铁的反应中,放出的热量能使铁熔化
科目:高中化学 来源: 题型:
根据物质的组成和性质将下列无机化合物进行了分类。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②______ | ③NaO ④______ | ⑤Na2SO4 ⑥______ | ⑦SO2 ⑧Na2O | ⑨HCl ⑩_____ |
(1)请仔细观察表格中的物质类别,从K、H、O、C、N五种元素中任选两种或三种组成合 适的物质,将化学式分别填在表中②、④、⑥、⑩后面的横线上。
适的物质,将化学式分别填在表中②、④、⑥、⑩后面的横线上。
(2)⑦和⑧可发生非氧化还原反应,生成一种盐。该反应的化学方程 式为_______________________________________________________
式为_______________________________________________________ _________________。
_________________。
(3)将⑦通入③的溶液中,反应的离子方程式为______________ ___________________
___________________
________________________________________________________________________。
(4)⑨极易溶于水并电离出氯离子,大多数含氯离子的盐溶于水后也能电离出氯离子。 检验溶液中 氯离子的方法是______________________________________________________________。
氯离子的方法是______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
A . 分液、蒸馏、萃取 B. 萃取、蒸馏、分液
C . 分液、萃取、蒸馏 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A.硝酸银溶液中滴加过量氨水:Ag++NH3·H2O===AgOH↓+NH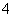
B.FeSO4溶液在空气中变质:4Fe2++O2+2H2O===4Fe3++4OH-
C.泡沫灭火器工作时化学反应: 2Al3++3CO32-+3H2O===2Al(OH)3↓+3CO2↑
D.过量碳酸氢钠溶液与氢氧化钡溶液反应:Ba2++2OH-+2HCO3-===BaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂。已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置制备亚氯酸钠。

完成下列填空:
(1)装置①中除烧杯外另一种玻璃仪器的名称为 。
(2)先关闭K1、打开K2、再打开分液漏斗旋塞,装置②中产生ClO2的化学方程式为 。
(3)当④中出现晶体后,则装置④中的化学反应方程式为 。然后关闭K2、打开K1,装置①的作用 。
将装置④中的溶液进行下列操作得到的晶体为NaClO2的操作步骤为:
①减压,55℃蒸发结晶; ② ;
③用38-60℃的温水洗涤 ④低于60℃干燥,得到成品。
(4)称取1g所得亚氯酸钠样品于烧杯中,加过量酸化碘化钾溶液,充分反应
(ClO2-+ 4I -+4H+ →2H2O+2I2+Cl-),得到25.00ml混合溶液。再用2.0 mol/L Na2S2O3标准液滴定(I2 +2S2O32-→2I-+S4O62-),共消耗Na2S2O3 20.00ml。
①滴定时指示剂为 ,达到滴定终点的现象为 。
②该样品中NaClO2的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有NH4+、SO32-、SiO32-、Br - CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的有NH4+、Na+ ②有胶状物质生成
③有气体产生 ④溶液颜色发生变化 ⑤共发生了2个氧化还原反应
A.①②③④ B.②③④ C.①③⑤ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3,关于该物质的说法正确的是( )
A.该物质属于两性氢氧化物 B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗3 mol H+ D.该药剂不适合于胃溃疡患者服用
查看答案和解析>>
科目:高中化学 来源: 题型:
已知化学反应A2(g) + B2(g) = 2AB(g)的能量变化如图所示,
判断下列叙述中正确的是
A.每生成2分子AB吸收b kJ热量
B.该反应热△H=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1molA—A和1molB—B键,放出a kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com