
【题目】已知2SO2(g) + O2(g) ![]() 2SO3(g) + Q kJ(Q>0)。在10 L恒温恒容密闭容器中加入0.1 mol SO2和0.05 mol O2,经过2 min达到平衡状态,反应放热0. 025 Q kJ。下列判断正确的是
2SO3(g) + Q kJ(Q>0)。在10 L恒温恒容密闭容器中加入0.1 mol SO2和0.05 mol O2,经过2 min达到平衡状态,反应放热0. 025 Q kJ。下列判断正确的是
A.在2 min内,O2的转化率为25%
B.在1min时,c(SO2) + c(SO3) = 0.01 mol/L
C.若再充入0.1 mol SO3,达到平衡后SO3的质量分数会减小
D.向该容器中再加入0.1 mol SO2和0.05 mol O2,平衡后反应放热大于0.05Q kJ
【答案】BD
【解析】
A. 根据热化学方程式知,1molO2完全反应放出Q kJ热量,则反应放热0. 025 QkJ时,反应的O2为0.025mol,则在2 min内,O2的转化率为![]() ,故A错误;
,故A错误;
B. 根据S原子守恒,反应过程中,c(SO2) + c(SO3) = ![]() ,故B正确;
,故B正确;
C. 若再充入0.1 mol SO3,平衡逆向移动,但达到平衡后SO3的质量分数会增大,故C错误;
D. 向该容器中再加入0.1 mol SO2和0.05 mol O2,若此时平衡与原平衡等效,则放出热量为0.05Q kJ,根据平衡移动原理,此时平衡正向移动,则平衡后反应放热大于0.05Q kJ,故D正确;
故选BD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
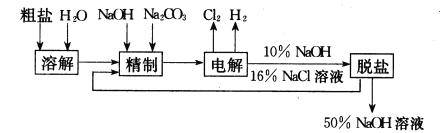
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应式为__________。 与电源负极相连的电极附近,溶液pH ________(选填:不变,升高或下降)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为___________,
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是______。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为 _________。
a. 先加NaOH,后加Na2CO3,再加钡试剂
b. 先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、_________(填写操作名称)除去NaCl。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物E的合成路线如图:
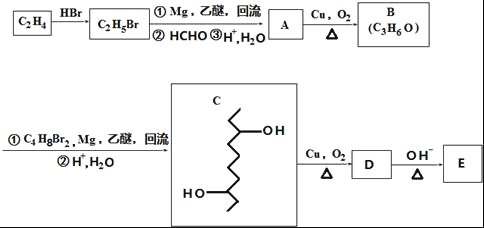
已知:
①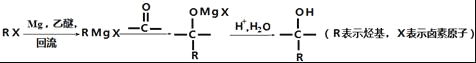
②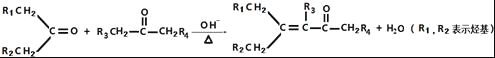
完成下列填空:
(1)B中官能团的名称为_____.C2H4生成C2H5Br的反应类型为____.
(2)C的分子式为_____.
(3)检验C2H5Br分子中含有溴原子的实验方案为____.
(4)E的结构简式为![]() ,D在一定条件下转变为E的过程中还会生成另两种具有五元环结构的副产物,写出这两种副产物结构简式_____.
,D在一定条件下转变为E的过程中还会生成另两种具有五元环结构的副产物,写出这两种副产物结构简式_____.
(5)写出一种满足下列条件的有机物的结构简式_____
①分子式只比E少2个氢原子
②与FeCl3发生显色反应
③分子中含有4种不同化学环境的氢原子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
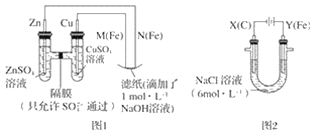
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__(填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__(填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种信息材料的添加剂,在相同条件下,A蒸气是同体积氢气质量的88.25倍。在A分子中各元素质量分数分别为w(C)=54.4%,w(H)=7.4%,w(O)=18.1%,w(Cl)=20.1%,A在不同条件下可发生如图所示的一系列变化。
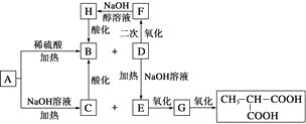
请回答下列问题:
(1)A的分子式为__________。
(2)D分子含有的官能团是________________。
(3)上述转换关系的化学方程式中,属于水解反应的有________个(填数字)。
(4)写出化学方程式:
①A和稀硫酸共热:____________________________________________________;
②E氧化成G:__________________________________________________;
③F与氢氧化钠醇溶液共热:__________________________________________。
(5)与B互为同分异构体的且属于链状酯的物质共有____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽油不仅是最重要的燃料,而且是重要的化工原料,它既可以裂解得到气态化工原料如乙烯等,还可以在催化剂催化下改变分子结构,由链烃变成芳香烃,如己烷变成苯,庚烷变成甲苯等。又知丙烯的化学性质和乙烯相似,请根据如图,回答有关问题:
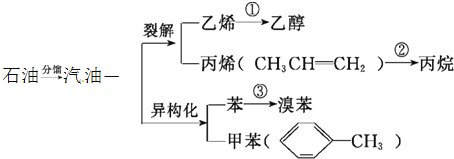
(1)写出相应的化学方程式:
![]() ______;
______;
![]() ______;
______;
![]() ______;
______;
(2)甲苯分子里苯环上一个氢原子被硝基取代后的产物有 ______ 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置可以在铜牌表面电镀一层银。下列有关说法正确的是( )

A.通电后,电解质溶液中的电子由阳极移到阴极
B.铜牌与电源正极相连
C.该电解池的阴极反应可表示为Cu2++2e-=Cu
D.当电镀一段时间后,电解质溶液中c(Ag+)保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.2 mol·L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.酸式滴定管准确量取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2~3次
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2~3mL处
E.调节液面至“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准氢氧化钠溶液滴定至终点并记下滴定管的读数
回答下列问题:
(1)正确的操作顺序是:B、_______________、F(填序号)
(2)滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 20.20mL | 38.80mL |
根据以上数据可以计算出盐酸的物质的量浓度为_______________mol·L-1. (计算结果小数点后保留两位有效数字)
(3)达到滴定终点的标志是________________________________
(4)以下操作造成测定结果偏高的原因可能是___________________。
A. 取待测液时,未用待测夜润洗酸式滴定管
B. 滴定前读数时,俯视滴定管的刻度,其它操作均正确
C. 滴定管滴定前无气泡,滴定后有气泡
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金、银、铜、铁、铝和钛均是人类生产和生活中大量使用的金属。试回答与上述金属原子结构有关的问题:
(1)上述金属元素中属于主族元素的有______。
(2)钛被称为继铁、铝之后的“第三金属”。基态钛原子外围电子排布图为______。
(3)基态金原子的外围电子排布式为![]() ,试判断金在元素周期表中位于第______周期第______族。
,试判断金在元素周期表中位于第______周期第______族。
(4)已知![]() 与
与![]() 位于同一族,则
位于同一族,则![]() 在元素周期表中位于______区。
在元素周期表中位于______区。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com