
将0.4molMg、Al的混合物用盐酸完全溶解,放出标况下11.2L气体,然后再投入一定量Na2O2固体,若该混合物与盐酸恰好完全反应,欲使最终沉淀为纯净物,则所加入Na2O2固体的质量为多少?
46.8g
(若算出Mg和Al的物质的量分别都为0.2moL给3分,全部解对7分。若过程中没有过程只有正确的结果只能给2分。) (解题过程,供参考)
Mg + 2HCl = MgCl2 + H2↑, 2Al + 6HCl = 2AlCl3 + 3H2↑,
2Na2O2 + 2H2O = 4NaOH + O2↑, MgCl2 + 2NaOH = Mg(OH)2↓ + 2NaCl,
AlCl3 + 4NaOH = NaAlO2 + 3NaCl + 2H2O。
(欲使沉淀为纯净物,则Al3+必须转化为AlO2-进入溶液。)
设混合物中Mg为Xmol,Al为Ymol:
由上述前两个反应知产生H2为X+3/2Y=11.2÷22.4=0.5,且混合物总的物质的量为X+Y=0.4。解得:X=0.2,Y=0.2。
再根据后三个方程式得:需要Na2O2为X+2Y=0.6,质量为0.6mol×78g/mol=46.8g。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
对下列化学用语的理解和描述不正确的是
A.原子结构示意图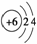 可以表示12C原子的,也可以表示14C原子的。
可以表示12C原子的,也可以表示14C原子的。
B.比例模型 可以表示二氧化碳分子,也可以表示水分子。
可以表示二氧化碳分子,也可以表示水分子。
C.结构示意图为 的阳离子都不能破坏水的电离平衡。
的阳离子都不能破坏水的电离平衡。
D.电子式 可以表示羟基,不可以表示氢氧根离子。
可以表示羟基,不可以表示氢氧根离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别
为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
A.(4c+12b-6a-5d)kJ·mol—1 B.(6a+5d-4c-12b)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1 D.(4a+5d-4c-12b)kJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.氧化铝既能和盐酸反应又能和氢氧化钠溶液反应均生成盐和水,说明氧化铝是两性氧化物。
B.NaHCO3的热稳定性比Na2CO3强
C.过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+
D.氯气中含有的少量氯化氢可用氢氧化钠溶液除去
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应并不改变的是
A.Na和O2 B.H2S和O2
C.Fe和FeCl3 D.AlCl3和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在氢氧化钙的悬浊液中,存在氢氧化钙固体与其电离出的离子间溶解结晶平衡:Ca(OH)2(s)  Ca2+(aq)+2OHˉ(aq)。向此种悬浊液中加入少量的氧化钙粉末,充分反应后恢复到原温度。下列叙述正确的是
Ca2+(aq)+2OHˉ(aq)。向此种悬浊液中加入少量的氧化钙粉末,充分反应后恢复到原温度。下列叙述正确的是
A.溶液中钙离子数目减小 B.溶液中钙离子浓度减少
C.溶液中氢氧根离子浓度增大 D.pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是
A.此腐蚀过程有化学腐蚀也有电化学腐蚀
B.发生电化学腐蚀时的正极反应为2H2O+O2+4e-=4OH-
C.在化学腐蚀过程中有氢气产生
D.发生电化学腐蚀时的负极反应为Fe=Fe2++2e-
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH <0,在其他条件不变的情况下( )
CO2(g)+H2(g) ΔH <0,在其他条件不变的情况下( )
A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
用10ml 0.1mol/L的BaCl2溶液恰好使相同体积的硫酸铁、硫酸锌和硫酸钠三种溶液的SO42-完全转化为BaSO4沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A.3∶2∶2 B.1∶2∶3 C.1∶3∶3 D.3∶1∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com