
 CO2↑+2SO2↑+2H2O ,A与B的组合是C、浓H2SO4; (3)若A、C均含有铝元素。①当B是盐酸时,则发生反应:NaAlO2+4HCl=NaCl+AlCl3+2H2O。则C是AlCl3。②当B是NaOH时,发生反应: AlCl3+4NaOH= NaAlO2+ NaCl+2H2O。C是NaAlO2.
CO2↑+2SO2↑+2H2O ,A与B的组合是C、浓H2SO4; (3)若A、C均含有铝元素。①当B是盐酸时,则发生反应:NaAlO2+4HCl=NaCl+AlCl3+2H2O。则C是AlCl3。②当B是NaOH时,发生反应: AlCl3+4NaOH= NaAlO2+ NaCl+2H2O。C是NaAlO2.

科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:Na2CO3<NaHCO3 |
| B.相同温度下在水中的溶解度:Na2CO3<NaHCO3 |
| C.等质量的两种固体,分别与过量盐酸反应,生成CO2的质量相等 |
| D.取1mol?L-1的两种溶液,分别滴入酚酞,溶液颜色较深的是Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.9mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 操作 | 解释或结论 |
| A | 向某溶液中加入NaOH溶液,出现白色沉淀 | 溶液中一定含有Mg2+ |
| B | 在饱和的SO2溶液中通入NO2气体,溶液的pH变小 | SO2具有还原性 |
| C | 某酸HX稀释100倍后,pH增加2 | HX是强酸 |
| D | 配制FeSO4溶液时,应加入过量铁粉和稀硫酸 | 溶液中不断产生FeSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
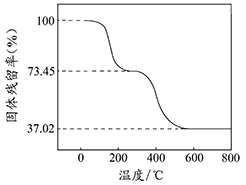
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c > b > d > a | B.b > a > d > c | C.a > b > c > d | D.d > c > b > a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| A.硬度比钢小,熔点比钢高 | B.不能与盐酸反应 |
| C.与不锈钢成分相同 | D.在冷的浓硫酸中钝化 |
 6Cu+SO2↑,该反应的氧化剂是
6Cu+SO2↑,该反应的氧化剂是 
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al2O3熔点很高,可用作耐火材料 |
| B.高纯度的硅单质用于制作光导纤维 |
| C.铝热反应是炼铁最常用的方法 |
| D.N2与O2在放电条件下直接化合生成NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com