
| 6-2×4+2 |
| 2 |


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
 超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:
超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:
2- 3 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

| 2-3 |
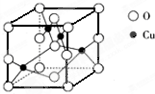
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键 |
| B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有大量NH3分子 |
| C.[Cu(NH3)4]SO4的组成元素中第一电离能最大的是氧元素 |
| D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都市彭州中学高二(上)期末化学试卷(解析版) 题型:解答题

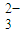 离子中S硫原子的杂化方式为______,与其互为等电子体的一种分子的分子式是______.
离子中S硫原子的杂化方式为______,与其互为等电子体的一种分子的分子式是______.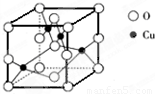
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com