
| A. | x的原子半径大于y的原子半径 | |
| B. | x的第一电离能小于y 的第一电离能 | |
| C. | x阴离子的半径小于y阳离子的半径 | |
| D. | x的电负性大于y的电负性 |
分析 x元素的阴离子和y元素的阳离子具有相同的电子层结构,离子核外电子数目相等,则y元素处于x元素的下一周期,x为非金属元素,最外层电子数较多,y为金属元素,最外层电子数相对较少,据此分析.
解答 解:x元素的阴离子和y元素的阳离子具有相同的电子层结构,离子核外电子数目相等,则y元素处于x元素的下一周期,x为非金属元素,最外层电子数较多,y为金属元素,最外层电子数相对较少,
A.y元素处于x元素的下一周期,电子层越多,半径越大,故原子半径y>x,故A错误;
B.x为非金属元素,y为金属元素,故x的第一电离能大于y的第一电离能,故B错误;
C.核外电子排布相同的离子,原子序数越大,离子半径越小,所以x阴离子的半径大于y阳离子的半径,故C错误;
D.x为非金属元素,y为金属元素,故x的电负性高于y的电负性,故D正确;
故选D.
点评 本题考查结构与位置的关系、半径与电负性、第一电离能比较等,题目难度不大,关键是根据离子具有相同的电子层结构推断元素的相对位置,侧重于考查学生的分析能力.


科目:高中化学 来源: 题型:解答题
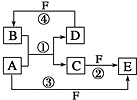 A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层电子排布为ns2的元素一定处于周期表IIA族 | |
| B. | 互为手性异构体的分子互为镜像 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 在晶体中有阳离子一定就有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与Fe、Br2混合 | B. | 氯乙烷和NaOH溶液共热 | ||
| C. | 溴乙烷和NaOH的乙醇溶液共热 | D. | 乙烯和溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷(乙炔):通过盛酸性高锰酸钾溶液的洗气瓶 | |
| B. | 乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热 | |
| C. | 苯(苯酚):加入NaCl溶液,然后分液 | |
| D. | 乙醇(水):加入生石灰,然后蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com