
分析 (1)[Fe(C2O4)3]3-为络离子,命名配离子时,配位体的名称放在前,中心原子名称放在后,配位体和中心原子的名称之间用“合“字相连;
(2)草酸被H2O2氧化生成水和二氧化碳;
(3)K3[Fe(C2O4)3]•3H2O中的铁为亚铁离子,而铁离子遇KSCN溶液变为血红色;
(4)A→KCN+Fe3C+C+N2,n(N2)=0.1mol,n(Fe3C)=0.1mol×$\frac{1}{3}$,n(C)=$\frac{0.1mol×\frac{1}{3}×180g/mol×\frac{1}{3}}{12g/mol}$=$\frac{1}{6}$mol,n(KCN)=$\frac{36.8g-0.1mol×28g/mol-6g-2g}{65g/mol}$=0.4mol,确定原子个数比得出化学式.
解答 解:(1)[Fe(C2O4)3]3-为络离子,命名配离子时,配位体的名称放在前,名称为:三草酸合铁(Ⅲ)离子(或三草酸合铁离子,或三草酸合铁酸根),
故答案为:三草酸合铁(Ⅲ)离子(或三草酸合铁离子,或三草酸合铁酸根);
(2)草酸被H2O2氧化生成水和二氧化碳,该反应为H2C2O4+H2O2=2CO2↑+2H2O,
故答案为:H2C2O4+H2O2=2CO2↑+2H2O;
(3)K3[Fe(C2O4)3]•3H2O中的铁为亚铁离子,则不能用KSCN溶液检验K3[Fe(C2O4)3]•3H2O中的铁元素,检验铁元素的方案为取适量晶体加热,取固体残留物溶解在H2SO4中,取上层清液于试管中,滴加KSCN溶液.若溶液呈血红色则有铁元素,反之则无,
故答案为:否;取适量晶体加热,取固体残留物溶解在H2SO4中,取上层清液于试管中,滴加KSCN溶液,若溶液呈血红色则有铁元素,反之则无;
(4)由题意可知,A→KCN+Fe3C+C+N2,n(N2)=0.1mol,Fe3C物质的量是氮气物质的量的$\frac{1}{3}$,n(Fe3C)=0.1mol×$\frac{1}{3}$,Fe3C质量是C质量的3倍,n(C)=$\frac{0.1mol×\frac{1}{3}×180g/mol×\frac{1}{3}}{12g/mol}$=$\frac{1}{6}$mol,n(KCN)=$\frac{36.8g-0.1mol×28g/mol-6g-2g}{65g/mol}$=0.4mol,则K、Fe、C、N的原子个数比为4:1:6:6,则化学式为K4Fe(CN)6,
故答案为:K4Fe(CN)6.
点评 本题考查知识点较多,涉及反应的配平、氧化还原反应、离子的检验及化学式的确定,(4)中注意利用守恒来解答,培养学生分析问题,解决问题的能力,题目难度中等.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 1、2-二溴乙烷可作汽油抗爆剂,常温下它是无色液体,密度2.18g/cm3,沸点131.4 0C,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室可以用下图所示装置制备1、2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管c中装有浓溴水.
1、2-二溴乙烷可作汽油抗爆剂,常温下它是无色液体,密度2.18g/cm3,沸点131.4 0C,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室可以用下图所示装置制备1、2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管c中装有浓溴水.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 仪器标号 | (1) | (2)(上) | (2)(下) | (3) | (4) | (5) |
| 试剂标号 | G | F |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知苯甲酸乙酯的沸点为213℃(在此温度以下水、乙醇和环己烷以7.0%、17.0%、76.0%的比例成为蒸汽逸出).请回答上述实验室制备苯甲酸乙酯的有关问题:
已知苯甲酸乙酯的沸点为213℃(在此温度以下水、乙醇和环己烷以7.0%、17.0%、76.0%的比例成为蒸汽逸出).请回答上述实验室制备苯甲酸乙酯的有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
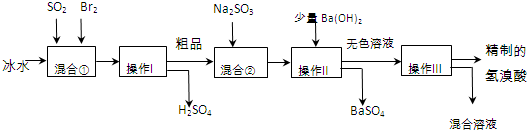
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氧化氯泡腾片,有效成分(ClO2)是一种高效、安全的杀菌、消毒剂.
二氧化氯泡腾片,有效成分(ClO2)是一种高效、安全的杀菌、消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.43×104 kJ | B. | 2.35×104 kJ | C. | 2.23×104 kJ | D. | 2.14×104 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com