
【题目】(1)已知甲烷的燃烧热是890 kJ/mol,且1 mol H2O由气态变为液态时放出44 kJ的能量。请写出甲烷燃烧生成水蒸气的热化学反应方程式为:____________________________;
(2)由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中作正极的是__________________ (填“A”或“B”) ;
②装置乙溶液中C电极反应:__________________________________;
③装置丙中金属A上电极反应属于______________(填“氧化反应”或“还原反应”);
④四种金属活动性由强到弱的顺序是___________________________。
【答案】 CH4(g)+2O2(g)==CO2(g)+2H2O(g) ΔH=-802 KJ/mol B Cu2++2e-==Cu 还原反应 D>A>B>C
【解析】(1)燃烧热是指在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量。根据题意可知,1mol甲烷完全燃烧生成2mol液态水,放出的热量是890kJ。而2mol液态水变成气态水又吸收44kJ×4=176kJ,所以甲烷燃烧生成水蒸气的反应热是(890+176)kJ/mol=802kJ/mol,因此热化学方程式为:CH4(g)+2O2(g)==CO2(g)+2H2O(g) ΔH=-802 kJ/mol;(2)①该装置中,金属A不断溶解说明A失电子发生氧化反应生成金属阳离子进入溶液而作负极,则作正极的是B,答案选B;②乙装置中,C的质量增加说明C电极上铜离子得电子发生还原反应,则C作正极,电极反应式为Cu2++2e-═Cu;③丙装置中A上有气体产生,说明A上氢离子得电子发生还原反应而作正极,正极上氢离子得电子发生还原反应;④通过以上分析知,四种金属活动性强弱顺序是D>A>B>C。


科目:高中化学 来源: 题型:
【题目】具有下列电子排布式的原子中,半径最大的是
A. ls22s22p63s23p2 B. 1s22s22p3 C. 1s22s2sp2 D. 1s22s22p63s23p4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容条件下可逆反应N2(g)+3H2(g) ![]() 2NH3(g),下列能够说明反应已经达到平衡状态的是
2NH3(g),下列能够说明反应已经达到平衡状态的是
A. c(N2)∶c(H2)∶c(NH3)=1∶3∶2
B. 氨气的百分含量不在变化
C. 断开一个N≡N键的同时有6个N—H键生成
D. 混合气体的质量不随时间的变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定石灰石样品中碳酸钙(含SiO2杂质)的含量。现利用下图所示装置进行实验,充分反应后,测定装置C中生成的BaCO3沉淀质量。下列说法正确的是
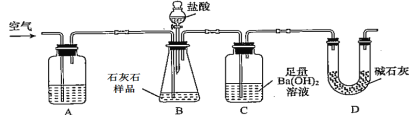
A.装置A中药品应为浓硫酸
B.在B—C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体
C.为了测得C中生成的沉淀质量,需经过过滤、洗涤、干燥、称量等操作
D.只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青菜含有维生素C和植物纤维有助于清除人体吸入的粉尘颗粒。已知维生素C的结构如图所示,有关判断不正确的是

A. 维生素C中含有3种官能团
B. 维生素C分子式为C6H8O6
C. 维生素C能使酸性高锰酸钾溶液褪色
D. 维生素C在碱性溶液中能稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液态溴。向a中滴入几滴溴,a中液体立即沸腾,并有红棕色蒸气出现;a中发生的化学方程式为;继续滴加至液溴滴完。仪器a的名称是装置d中的作用是。仪器c为冷凝管,其进水口为(填“上”或“下”)口。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是。
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为 , 要进一步提纯,下列操作中必须的是。
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据价层电子对互斥理论及原子的杂化轨道理论判断NF3分子的空间构型和中心原子的杂化方式为( )
A. 直线形 sp杂化 B. 三角形 sp2杂化
C. 三角锥型 sp2杂化 D. 三角锥型 sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )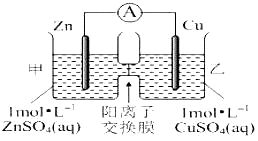
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的C(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阳离子通过交换膜向正极移动,阴离子通过交换膜向负极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下图装置制备家用消毒液,并探究其性质。
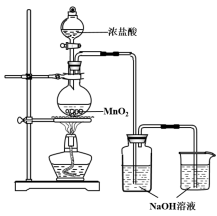
反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
a. 测溶液pH, 并向其中滴加2滴酚酞 | pH = 13, 溶液变红,5min后褪色 |
b. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(1)写出利用上述装置制备消毒液涉及反应的化学方程式 、 。
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作a中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有 性。
(3) 该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降。
① 操作b中溶液变成黄绿色的原因: (用离子方程式表示)。
② 有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是 。
(4) 有效氯的含量是检测含氯消毒剂消毒效果的重要指标。具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上。小组同学进行如下实验测定有效氯:取此消毒液5 g,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液;加几滴淀粉溶液后,用0.1 mol·L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3 20 mL。(已知:2S2O32- + I2 === S4O62- + 2I-) 。注:相对原子质量Cl35.5,Na23,S32,O 16 ,I 127, K39
①达到滴定终点时的实验现象是 。
②此消毒液有效氯含量为 %(保留一位有效数字)。获得结论:此实验制得的消毒液 (填“符合”或“不符合”)家用要求。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com