
【题目】已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间以单键结合。下列有关C3N4晶体的说法中错误的是
![]()
A.C3N4晶体与金刚石都属于原子晶体
B.C3N4晶体中C-N键的键长比金刚石中的C-C键的键长长
C.C3N4晶体中每个碳原子连接4个氮原子,每个氮原子连接3个碳原子
D.C3N4晶体中含有极性共价键,不含非极性共价键
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】化合物H是一种有机材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①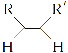
![]() RCHO+R′CHO
RCHO+R′CHO
②RCHO+R′CH2CHO![]()
![]() +H2O
+H2O
③![]()
请回答下列问题:
(1)芳香族化合物B的名称为________,1molB最多能与_____molH2加成,其加成产物等效氢共有_______种。
(2)由E生成F的反应类型为________,F分子中所含官能团的名称是_______。
(3)X的结构简式为________。
(4)写出D生成E的第①步反应的化学方程式______。
(5)G与乙醇发生酯化反应生成化合物Y,Y有多种同分异构体,其中符合下列条件的同分异构体有________种,写出其中任意一种的结构简式____。
①分子中含有苯环,且能与饱和碳酸氢钠溶液反应放出CO2;②其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1。
(6)根据题目所给信息,设计由乙醛和苯甲醛制备![]() 的合成路线(无机试剂任选)______。
的合成路线(无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2一二氯丙烷(CH2ClCHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3一氯丙烯(CH2=CHCH2Cl),反应原理为:
i .CH2 =CHCH3(g) +C12(g)CH2ClCHClCH3(g) △H1=-134kJmol-1
ii . CH2 =CHCH3(g) +C12(g)CH2= CHCH2Cl(g) +HCl(g) △H2 =-102kJmol-1
请回答下列问题:
(1)已知:CH2 =CHCH2Cl (g) + HCl ( g)CH2ClCHClCH3(g)的正反应的活化能Ea(正)为132 kJmol-1,则逆反应的活化能Ea(逆)为__________ kJmol-1 。
(2)某研究小组向密闭容器中充入一定量的C12(g)和CH2 =CHCH3 ( g),分别在 A、B两种不同催化剂作用下发生反应,一段时间后测得CH2ClCHClCH3的产率与温度的关系如图1所示。
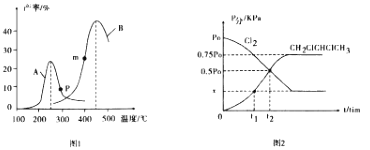
①下列说法正确的是______(填代号)。
a .使用催化剂A、B的最佳温度:A <B
b .p、m点分别是对应温度下CH2ClCHClCH3的平衡产率
c. 使用催化剂降低了反应的活化能和焓变
d. 温度不变,增大压强可使CH2ClCHClCH3的产率提高
②在250℃以后,A曲线中产率下降的原因可能是________(写出两条)。
(3)T℃时使用选择性更高的催化剂,在恒容密闭容器内充入等物质的量的C12 ( g) 和CH2=CHCH3 (g)进行反应i,测得容器各组分的分压强(p分=p总×体积分数)随时间的变化关系如图2所示,回答下列问题:
①若用单位时间内气体分压的变化来表示反应速率,即υ= ![]() ,则t1~t2时间段内平均反应速率υ(CH2=CHCH3)= _______ kPamin-1(用相关字母表示);平衡时CH2ClCHClCH3的体积分数________。
,则t1~t2时间段内平均反应速率υ(CH2=CHCH3)= _______ kPamin-1(用相关字母表示);平衡时CH2ClCHClCH3的体积分数________。
②反应的平衡常数KP=_____________(用平衡分压代替平衡浓度,相关字母表示结果)。
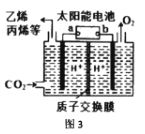
(4)如图3是在酸性电解质溶液中,用惰性电极将CO2转化为低碳烯烃的电化学装置,回答下列问题:
①太阳能电池的负极是 __________(填“a”或“b”)。
②生成丙烯的电极反应式是____________。
③相同时间内,相同条件下,消耗的CO2与生成的O2 的体积之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】线型 PAA( ![]() )具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
)具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
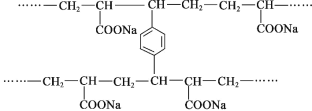
A.线型 PAA 的单体不存在顺反异构现象
B.形成网状结构的过程发生了加聚反应
C.交联剂 a 的结构简式是![]()
D.PAA 的高吸水性与—COONa 有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示,下列叙述错误的是
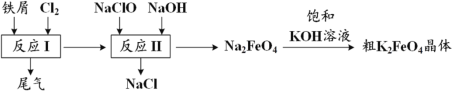
A.用 K2FeO4 作水处理剂时,既能杀菌消毒又能净化水
B.反应 I 中尾气可用 FeCl2 溶液吸收再利用
C.反应 II 中氧化剂与还原剂的物质的量之比为 2:3
D.该条件下,物质的溶解性:Na2FeO4< K2FeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水垢中含有的 CaSO4,可先用 Na2CO3 溶液处理,使之转化为疏松、易溶于酸的 CaCO3。某化学兴 趣小组用某浓度的 Na2CO3 溶液处理一定量的 CaSO4 固体,测得所加 Na2CO3 溶液体积与溶液中-lgc(CO32-) 的关系如图所示,已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是
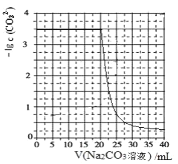
A.曲线上各点的溶液满足关系式:c(Ca2+)×c(SO42-)=Ksp(CaSO4)
B.CaSO4(s)+CO32-(aq) ![]() CaCO3(s)+SO42-(aq) K=3×103
CaCO3(s)+SO42-(aq) K=3×103
C.该Na2CO3溶液的浓度为1.5mol·L-1
D.相同条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则上图曲线整体向上平移1个单位即可
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的循环寿命,放电时的反应为:LixC6+Li1-xFePO4=6C+LiFePO4-。某磷酸铁锂电池的切面如图所示。下列有关说法错误的是

A.放电时,Li+脱离石墨,该过程中碳元素化合价发生了变化
B.在周期表中,与Li的化学性质最相似的邻族元素是Mg,其基态原子核外M层的两个电子自旋状态相反
C.PO43-的水解方程式为PO43-+3H2OH3PO4+3OH-
D.石墨属于混合晶体,层与层之间存在分子间作用力,层内碳原子间存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C. 1 mol Fe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的的是
A | B | C | D | |
实验目的 | 实验室制乙酸乙酯 | 比较碳酸与苯酚酸性强弱 | 加入CCl4分离碘水中的碘 | 蒸干FeCl3溶液制无水FeCl3 |
实验装置 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com