
����(H3BO3)��Һ�д������·�Ӧ��H3BO3(aq)��H2O(l)  ?[B(OH)4]��(aq)��H��(aq)������˵����ȷ����
?[B(OH)4]��(aq)��H��(aq)������˵����ȷ����
��ѧʽ | ���볣��(298 K) |
H3BO3 | K��5.7��10��10 |
H2CO3 | K1��4.4��10��7 K2��4.7��10��11 |
CH3COOH | K��1.75��10��5 |
A.��һ��̼������Һ����������Һ��һ���ܹ۲쵽�����ݲ���
B����һ�δ�����Һ����̼������Һ��һ���ܹ۲쵽�����ݲ���
C�������ʵ���Ũ�ȵ�̼����Һ��������Һ�Ƚϣ�pH��ǰ��>����
D�������ʵ���Ũ�ȵ�̼������Һ�ʹ�������Һ�Ƚϣ�pH��ǰ��>����
D
��������A������ݿ�֪����ͬ�����£�̼�������ǿ�����ᣬ��̼���������ᷴӦֻ������̼�����ƣ����ܵõ�CO2���壬����B���������ʱ��������̼������Һ��Ӧ���ɵ���̼�����ƺʹ����ƣ����ܲ������壬����C������ʵ���Ũ�ȵ�̼����Һ��������Һ��ǰ�ߵ�c (H��)��pH��С������D���ͬ�����£����������ǿ��̼�ᣬ����Խ��Խˮ����ɿ�֪�����������ӵ�ˮ��̶�С��̼������ӣ������ʵ���Ũ����ͬʱ��̼������Һ�ļ���ǿ�ڴ�������Һ����ȷ��


 ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д� ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��15 ���ͣ�ѡ����
ij�¶��£���������������Ϊa%��KOH��Һ������m gˮ��ָ���ԭ�¶ȣ�ǡ�õõ���������Ϊ2a%��KOH������ҺV mL��������˵������ȷ����
A�����¶���KOH���ܽ��Ϊ100a/(100��a)g
B��ԭ��Һ������Ϊ2m g
C����������ԭ��Һ�����ʵ���Ũ��
D�������¶Ȳ��䣬��ԭ��Һ�м���2a g KOH�ɴﱥ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ѡ����
���н��۲���ȷ����
A���Ӱ뾶��S��S2����Cl��
B�⻯��е㣺H2O��HF��HCl
C�������������OH����SiO��CO
D���ӻ�ԭ�ԣ�S2����I����Br��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��12 ���ͣ��ƶ���
���л��ﻯѧ������
ij�л���X����Է�������С��100,ȡ1 mol�л���X��O2����ȫȼ�����ɵ����ʵ�����CO2��H2O��ͬʱ���ı�״���µ�O2 112 L��
��1�����л���X�ķ���ʽΪ________������ţ���
A C4H8 B C2H4O C C4H8O2 D C10H20O20
��2����������X��ͬ���칹�壬�����к����ʻ����ǻ����������ܷ�����ͼ��ʾ��ת����
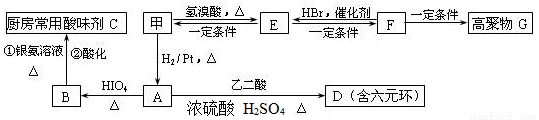

��B��������________����A��������ͬ��ͬ���칹�干��______�֣�����A�����������칹����֪ͬһ��̼���������ǻ����л��ﲻ�ȶ���
��A��D�ķ�Ӧ����Ϊ________��E��F�ķ�Ӧ������________��
��д��F��G�Ļ�ѧ����ʽ__________________________________��
��3��������Ҳ��X��ͬ���칹�壬1 mol����������Na��Ӧ������1 mol H2�����Ҳ���ʹ���CCl4��Һ��ɫ���ҷ����еĹ������������ڵ�̼ԭ���ϡ��ҵĺ˴Ź�������ͼ����3���壬���֮��Ϊ2��1��1�������ҵĽṹ��ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��12 ���ͣ�ѡ����
������Զ�������г���Ӧ��ԭ���ԭ���Ĵ���������ͼΪ��صĹ���ʾ��ͼ��������ɢ���봫�����������е缫�Ϸ�����Ӧ���������ͻ���յ����źš��±��г��˴������弰���е缫�ϲ��ַ�Ӧ���������˵������ȷ����
�������� | ���ֵ缫��Ӧ���� |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |

A������������ʱ�����е缫�����������
B�����Cl2����ʱ�����е缫�ĵ缫��ӦΪ��Cl2 + 2e��= 2Cl��
C�����H2S����ʱ���Ե缫����������Ե缫�ϵĵ缫��ӦʽΪO2 + 2H2O+ 4e�� = 4OH��
D�����H2S ��CO���������ͬ�����ݿ�������ʱ���������ϲ����ĵ�����С��ͬ
��CO���������ͬ�����ݿ�������ʱ���������ϲ����ĵ�����С��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��11 ���ͣ������
�������ڹ�ҵ�������й㷺����;��
��1��SO2�����ڹ�ҵ����SO3��
����һ�������£�ÿ����8g SO3���壬����9.83kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ________��
����500�棬�������ڵ������£����ݻ�Ϊ1L�ļס��������ܱ������о����� 2 mol SO2��1 mol O2���ױ���ѹǿ���䣬�ұ����ݻ����䣬��ַ�Ӧ����ﵽƽ�⡣
I��ƽ��ʱ����������SO3��������Ĺ�ϵΪ����_______�ң��>������<���� =������
II��������t1 minʱ�ﵽƽ�⣬��ʱ�����������SO2��ת����Ϊ90%�����
��Ӧ��ƽ�ⳣ��Ϊ_______�������¶Ȳ��䣬t2 minʱ����������г���1 mol SO2��1 mol SO3��t3minʱ�ﵽ��ƽ�⡣������ͼ�л���t2~t4 min�����淴Ӧ���ʵı仯���ߣ������ϱ������V����V�� ��

��2������þ���壨MgSO4��7H2O )���Ƹҽҩ��������й㷺��;��4.92g����þ����������ˮ���̵��������ߣ������������¶ȱ仯�����ߣ�����ͼ��ʾ��

�ٹ���M�Ļ�ѧʽΪ__________��
������þ��������ʧȥ�ᾧˮ�Ĺ��̷�Ϊ_________���Ρ�
��Nת����Pʱ��ͬʱ������һ��������÷�Ӧ�Ļ�ѧ����ʽΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��11 ���ͣ�ѡ����
���л�ѧ�����ʾ��ȷ����
A.��ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��2H2��g��+O2��g��= 2H2O��1����H= -571.6kJ/mol
B����������Ҫ�ɷ�ΪRCOONa����ˮ��Һ�Լ��ԣ�RCOO-+H2O RCOOH+OH-
RCOOH+OH-
C��ʵ���������������ӷ���ʽ��MnO2+4H++4Cl�� MnCl2+2H2O+Cl2��
MnCl2+2H2O+Cl2��
D���������Ҵ���Ӧ�Ļ�ѧ����ʽ��CH3CO18OH+C2H5OH CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��10 ���ͣ��ƶ���
���л��ﻯѧ������

�л���G���Ʊ�Һ�����ϵ��м���֮һ����ṹ��ʽΪ��

G��һ�ֺϳ�·�����£����У�A��F�ֱ����һ���л�������ϳ�·���еIJ��ֲ��P��Ӧ��������ȥ��
��֪��X�ĺ˴Ź�������ֻ��1�ַ壻RCH��CH2 RCH2CH2OH��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ�����ش��������⣺
RCH2CH2OH��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ�����ش��������⣺
��1��A�Ľṹ��ʽ�� ��C�й����ŵ������� ��
��2��B�������� ���ڢ١��߲�������ȡ����Ӧ���� ������ţ�
��3��д����Ӧ�ݵĻ�ѧ����ʽ ��
��4���ڢ߲���Ӧ�Ļ�ѧ����ʽ�� ��
��5��G���������õ�Y��C11H12O4����д��ͬʱ��������������Y������ͬ���칹��Ľṹ��ʽ ��
a.�����ϵ�һ�ȴ�����2�֣� b.ˮ�����ɶ�Ԫ����ʹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ�� ���ͣ�ѡ����
25 ��ʱ��0.1 mol/L��HA��Һ��c(H��)/c(OH��)��l��l06������������ȷ����
A������Һ����ˮ�������c(H��)��l��10��13 mol/L
B����pH��4��HA��pH��10��NaOH��Һ�������ϣ���Һ��c(Na��)>c(A��)>c(OHһ)>c(H��)
C. Ũ�Ⱦ�Ϊ0.1 mol/L��HA��NaA��Һ�������ϣ�����Һ�����ԣ���c(A��)��c(HA)��c(Na��)��c(H��)��c(OH��)
D��0.1 mol��L��1 HA��Һ��0.05 mol��L��1 NaOH��Һ�������Ϻ�������Һ��c(H��)��c(Na��)��c(OH��)��c(A��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com