
����Ŀ�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ�����������ʷ����ĵ缫��Ӧ����д������ش��������⣺
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
��д����ⱥ��NaCl��Һ�ܵ����ӷ���ʽ_____��
����X�������۲쵽��������_____������Y�缫��Ӧ����ķ�����_____��
��2����Ҫ�õ�ⷽ��������ͭ������п��������Ͳ��������ʣ������Һaѡ��CuSO4��Һ����
��X�缫�����ķ�Ӧ����Ϊ_____�����ӵ�������_____��_____����X��Y������Y�缫�IJ�����_____���缫��ӦʽΪ_____��CuSO4��Һ��Ũ��_____������䡱���������ӡ������м��١�����

���𰸡�2Cl��+2H2O![]() 2OH��+H2��+Cl2���ų����壬��Һ����ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��ԭ��ӦY��X��ͭCu��2e��=Cu2+ ��Zn��2e��Zn2+�� Fe��2e��Fe2+���м���
2OH��+H2��+Cl2���ų����壬��Һ����ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��ԭ��ӦY��X��ͭCu��2e��=Cu2+ ��Zn��2e��Zn2+�� Fe��2e��Fe2+���м���
��������
��1�����ö��Ե缫��ⱥ��ʳ��ˮʱ��������2Cl����2e��Cl2����������2H+��2e��H2�����ܷ�ӦΪ��2Cl��+2H2O![]() 2OH��+H2��+Cl2�����ʴ�Ϊ��2Cl��+2H2O
2OH��+H2��+Cl2�����ʴ�Ϊ��2Cl��+2H2O![]() 2OH��+H2��+Cl2������X��Ϊ�������缫��ӦΪ��2H+��2e��H2�����缫����������������Ũ����������ǿ�������۲쵽�������Ƿų����壬��Һ��죻Y��Ϊ�������缫��ӦΪ��2Cl����2e��Cl2������������ͨ����ʪ��ĵ⻯�ص�����ֽ�����飬�ʴ�Ϊ���ų����壬��Һ�������ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
2OH��+H2��+Cl2������X��Ϊ�������缫��ӦΪ��2H+��2e��H2�����缫����������������Ũ����������ǿ�������۲쵽�������Ƿų����壬��Һ��죻Y��Ϊ�������缫��ӦΪ��2Cl����2e��Cl2������������ͨ����ʪ��ĵ⻯�ص�����ֽ�����飬�ʴ�Ϊ���ų����壬��Һ�������ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
��2�����ڵ���װ������X�����Դ����������Ϊ������������ԭ��Ӧ����������Ϊ���������·����������Ϊ��Y��X���ʴ�Ϊ����ԭ��Ӧ�� Y��X�����ڵ�⾫��ͭ��װ���У���ͭΪ��������ͭΪ������������ӦΪ��Cu��2e��Cu2+������п������ͭ���ã�Ҳ����ŵ磬��Y�����ᷢ����Zn��2e��Zn2+�� Fe��2e��Fe2+����������ֻ��Cu2+��2e��Cu���ɵ�ɿ�֪CuSO4��Һ��Ũ�����м������ʴ�Ϊ��Cu��2e��=Cu2+ ��Zn��2e��Zn2+�� Fe��2e��Fe2+�����м�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩͪ�Ľṹ��ʽΪCH2��C��O����һ����Ҫ���л��м��壬���������������ˮ�õ�������˵������ȷ����
A. 1mol��ϩͪ��1molH2��ȫ��Ӧ����1mol�Ҵ�
B. ��ϩͪ�����е�ԭ�Ӿ�����ͬһƽ����
C. ��ϩͪ��ˮ��Ӧ��������ķ�Ӧ���ڼӳɷ�Ӧ
D. ��ϩͪ��![]() ��Ϊͬ���칹��
��Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ���������������ֶ�����Ԫ��(����ĸx�ȱ�ʾ)ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯����ͼ��ʾ��

�����жϳ���Ԫ�ػش����⣺
(1)f�����ڱ��е�λ����___________��
(2)�Ƚ�d��e�������ӵİ뾶��С(�û�ѧʽ��ʾ����ͬ)��______>______���Ƚ�g��h������������Ӧˮ���������ǿ����_______��
(3)д��һ�ּȺ����Ӽ��ֺ����Թ��ۼ�e��������ĵ���ʽ��_____��
(4)��֪1 gX�ĵ���������d2��ȼ�գ��ָ������£��ų�142.9kJ������д����ʾ��ȼ���ȵ��Ȼ�ѧ����ʽ��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��ӦA2(g)��B2(g)===2AB(g)�������仯��ͼ��ʾ���ж�������������ȷ����
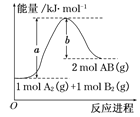
A. ÿ����2����AB����b kJ����
B. �÷�Ӧ����H����(a��b) kJ��mol��1
C. �÷�Ӧ�з�Ӧ��������������������������
D. ����1 mol A��A��1 mol B��B�����ų�a kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2L���ܱ������У�ij���淴Ӧ�ڲ�ͬ��Ӧʱ������ʵ����ı仯�����ͼ��ʾ��
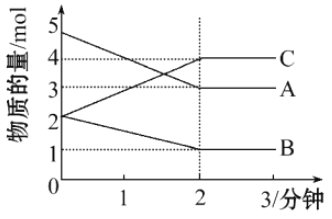
��1����÷�Ӧ�ĵķ�Ӧ����______����������_____��
��2���÷�Ӧ�Ļ�ѧ����ʽΪ___________��
��3���ӷ�Ӧ��ʼ��2����ʱ����C��ʾ�䷴Ӧ����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʶ�����Ư���ԣ�Ư��ԭ�����������ֲ�ͬ���ǣ� ��
A.��ˮB.SO2C.H2O2D.HClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ������и���ѧ����ͼ��ʾ�����й����Ҵ��ڲ�ͬ�ķ�Ӧ�ж��ѻ�ѧ����˵���������

A. ������Ʒ�Ӧʱ�����ٶ���
B. �ڼ��Ⱥ�Cu������O2��Ӧʱ�����١��۶���
C. ��Ũ���Ṳ�ȷ�����ȥ��Ӧʱ�����ڢ۶���
D. �����ᡢŨ���Ṳ�ȷ���������Ӧʱ�����ٶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ����������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ���
A. SiO2![]() SiCl4
SiCl4![]() Si
Si
B. FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C. N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
D. MgCO3![]() MgCl2(aq)
MgCl2(aq) ![]() Mg
Mg
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com