
【题目】碳铵是一种较常使用的化肥,它在常温下易分解。某化学兴趣小组对碳铵的成分存在疑问,时行了如下探究。
【定性实验】检验溶液中的阴、阳离子
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成.再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色.
(1)根据实验现象,推测碳铵中所含有阴离子可能是_______和_______;
(2)根据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是__________ __________;
【定量试验】测定碳铵中C元素和N元素质量比.该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如图所示.

(3)碳铵固体应放在________中进行加热.
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
(4)从安全的角度考虑,尾气处理的装置可以选用________;

(5)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg.由此测得N元素的质量是_____g。
(6)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量.请你评价该方案是否合理;________(填“合理”“不合理”),理由是________。
【答案】(1)HCO3-、CO32- (各1分,共2分)
(2)NH4++OH-![]() NH3↑+H2O 或NH4++HCO3-+2OH-
NH3↑+H2O 或NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O (2分)
NH3↑+CO32-+2H2O (2分)
(3)A(2分) (4)A(2分) (5)![]() (2分)
(2分)
(6)本小题属于开放性试题,若考生只回答“合理”或“不合理”不给分;若考生回答“合理”或“不合理”且理由能做出相应解释,可酌情给分(3分)。例如:考生回答
①不合理,因为碳铵中可能含有HCO3-,不能与BaCl2产生沉淀,所测得碳元素质量分数不准确。
②合理,因为碳铵中只含有CO32-,加入BaCl2能完全生成沉淀,可准确测得碳元素的质量”。
【解析】
试题分析:【定性实验】取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成,白色沉淀为碳酸钙,盐中阴离子可能HCO3-、CO32-;再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色,则气体为氨气,则原固体中含铵根离子,(1)由上述分析可知,阴离子可能为HCO3-、CO32-;(2)碳铵与足量NaOH溶液加热反应的离子方程式可能是NH4++OH-=NH3↑+H2O、HCO3-+OH-=CO32-+H2O(或NH4++HCO3-+2OH-=NH3+CO32-+2H2O);【定量实验】ag碳铵,加热使之分解,碱石灰增重为水和二氧化碳的质量,尾气处理为氨气,(3)因加热装置后连接U形管,则选择仪器只能为试管,故答案为A;(4)尾气处理,应防止倒吸,B不能防止倒吸,C中气体收集时导管应短进,D中为密闭容器可能会炸裂,只有A装置收集及防倒吸,故答案为A;(5)灼烧后没有固体残余,称量U形管在实验前后的质量差为bg,则氨气的质量为(a-b)g,则含N质量为![]() g;(6)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,则①不合理,因为碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确;②合理,因为碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量;③不合理;测得的结果不准确。
g;(6)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,则①不合理,因为碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确;②合理,因为碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量;③不合理;测得的结果不准确。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
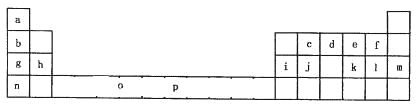
试回答下列问题:
(1)元素p为26号元素,请画出其基态原子外围电子排布图______________;
(2)e与a反应的产物的分子中中心原子的杂化形式为________________;该分子是_________(填“极性”或“非极性”)分子。
(3)上表中元素基态原子的第一电离最大的元素是__________。(用元素符号表示)
(4)o、p两元素的部分电离能数据列于下表:
元 素 | O | P | |
电离能 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难,对此,你的解释是______________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届邯郸一模】【化学选修3:物质结构与性质】
新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为_________,该能层具有的原子轨道数为________。
②LiBH4由Li+和BH4-构成,BH4-的立体结构是_________,B原子的杂化轨道类型是________。
Li、B、H元素的电负性由大到小排列顺序为________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径Li+_______H-(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
I1/kJmol-1 | I2/kJmol-1 | I3/kJmol-1 | I4/kJmol-1 | I5/kJmol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是________ (填元素符号)。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为________,NaH的理论密度是___________g·cm-3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
![]()

(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2 分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 (填序号)。
A.适当减缓通入Cl2速率
B.充分搅拌浆料
C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O氯化完成后过滤。

①滤渣的主要成分为 (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2] 1∶5(填“>”、“<”或“=”)。
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100gL-1,从该溶液中尽可能多地析出KClO3固体的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.由 D和18O所组成的水11g,所含中子数为4NA
B.1 L 0.4 mol·L-1稀硝酸与Fe完全反应,转移电子数为0.3NA
C.标准状况下,2.24LCHCl3所含分子数为 0.1NA
D.密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中所含的杂质,选用的试剂正确的是( )
选项 | 物质(杂质) | 试剂 |
A | Al2O3(SiO2) | NaOH溶液 |
B | FeCl2溶液(FeCl3) | Fe粉 |
C | CO2(SO2) | Na2CO3溶液 |
D | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。

完成下列填空:
(1)实验时,通常加入过量的乙醇,原因是______________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是_______________;浓硫酸用量又不能过多,原因是____________。
(2)饱和Na2CO3溶液的作用是_______________。
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,_________、________,然后分液。
(4)若用b装置制备乙酸乙酯,其缺点有__________、__________。由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________,分离乙酸乙酯与该杂质的方法是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛。
(1)Mg2Ni是一种储氢合金,已知:
Mg(s) + H 2 (g)=MgH 2 (s) △H 1 =-74.5kJ·mol -1
Mg 2 Ni(s) + 2H 2 (g)=Mg 2 NiH 4 (s) △H 2 =-64.4kJ·mol -1
Mg 2 Ni(s)+2MgH 2 (s) = 2Mg(s)+Mg 2 NiH 4 (s) △H 3
则△H 3 = kJ·mol -1 。
(2)工业上可用电解熔融的无水氯化镁获得镁。其中氯化镁脱水是关键工艺之一,一种正在试验的氯化镁晶体脱水的方法是:先将MgCl 2 ·6H 2 O转化为MgCl 2 ·NH 4 Cl·nNH 3,然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为 ;电解熔融氯化镁,阴极的电极反应式为 。
(3)储氢材料Mg(AlH4) 2 在110~200°C的反应为:Mg(AlH4) 2 =MgH 2 +2Al+3H 2 ↑每生成27gAl转移电子的物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某温度下,在2 L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t1 min时到达平衡,如图所示:

(1)该反应的化学方程式是 。
(2)①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol 氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为 ;在此t1 min时间内,用H2表示反应的平均速率v(H2)为 。
Ⅱ.亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式是:
Na2SO3+KIO3+H2SO4 = Na2SO4+K2SO4+I2+H2O,
该反应过程和机理较复杂,一般认为分为以下几步:
IO3-+SO32-→IO2-+SO42-(慢)②IO2-+ SO32-→IO-+SO42-(快)
③5I-+6H++ IO3-→3I2+3H2O(快)④I2+ SO32-+ H2O→2I-+ SO42-+2H2(快)
(1)根据上述条件推测,此反应的总的反应速率由 步反应决定。
(2)若预先加入淀粉溶液,由题述看必在 离子消耗完时,才会使淀粉谈蓝的现象产生。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com