
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 铅蓄电池在放电时,两极质量均增加 | |
| C. | 钢铁在中性溶液中主要繁盛析氢腐蚀 | |
| D. | 在室温下能自发进行的反应,其△H一定小于0 |
分析 A、在原电池中正极被保护;
B、根据铅蓄电池中的电极反应分析;
C、钢铁在酸性条件下发生析氢腐蚀;
D、反应自发进行的判断依据是△H-T△S<0.
解答 解:A、在海轮的外壳上镶入锌块,会和铁形成原电池,锌做负极,海轮做正极,而在原电池中正极被保护,故可减缓船体的腐蚀,故A正确;
B、放电时,铅失电子发生氧化反应而作负极,电极反应式为Pb-2e-+SO42-=PbSO4,二氧化铅得电子作正极,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,两极均生成难溶性的PbSO4,所以两极质量均增加,故B正确;
C、钢铁在酸性条件下发生析氢腐蚀,在中性或弱酸性条件下发生吸氧腐蚀,故C错误;
D、反应自发进行的判断依据是△H-T△S<0,在室温下能自发进行的反应,其△H不一定小于0,故D错误;
故选AB.
点评 本题考查了金属的电化学腐蚀及防护,难度不大,应注意的是在原电池中正极被保护,在电解池中阴极被保护.


 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{(N-M)}{45}$ | B. | $\frac{(M-N)}{45}$ | C. | $\frac{(M-N)}{90}$ | D. | $\frac{(N-M)}{90}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,22.4L C5H10所含的碳原子数目为5NA | |
| B. | 常温常压下,7.8g过氧化钠含有的离子数为0.3NA | |
| C. | 18g水所含的电子数目为10NA | |
| D. | 3.2g O2、O3混合物中所含氧原子一定是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
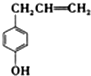
| A. | 该化合物属于芳香烃 | |
| B. | 1mol该化合物最多可与3molBr2发生反应 | |
| C. | 它的部分同分异构体能发生银镜反应 | |
| D. | 该化合物不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚与溴水可以直接反应,而苯与液溴反应则需要铁作催化剂 | |
| B. | 乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应 | |
| C. | 甲苯能使酸性KMnO4溶液褪色,而甲基环己烷不能使酸性KMnO4溶液褪色 | |
| D. | 苯酚可以与NaOH反应,而乙醇不能与NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
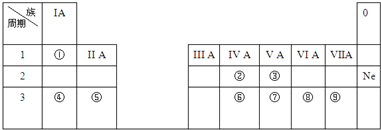
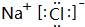 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 置换反应 | C. | 复分解反应 | D. | 氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石溶于稀盐酸:CaCO3+2H+═CO2↑+Ca2++H2O | |
| B. | 钠与冷水反应:Na+2H2O═Na++OH-+H2↑ | |
| C. | 铁与稀盐酸反应:Fe+2H+═H2↑+Fe2+ | |
| D. | 铝粉与氢氧化钠溶液反应:2Al+2H2O+2OH-═2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品保存在冰箱中不易坏,说明温度对反应速率有影响 | |
| B. | 在金属与非金属的分界线附近寻找半导体材料 | |
| C. | 在周期表中,第IA族全部为金属元素 | |
| D. | 金刚石与石墨互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com