
【题目】下列化学用语表示正确的是( )
A.乙酸的结构简式:C2H4O2
B.乙烯的电子式: ![]()
C.硫离子结构示意图: ![]()
D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH﹣)2
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】为测定某有机含氧化合物A的结构,通过实验得出以下数据: ①将有机化合物A置于氧气流中充分燃烧,实验测得生成5.4g H2O和8.8g CO2 .
②利用质谱仪测定出有机化合物A的相对分子质量为46.
③该有机物可与金属钠反应,生成氢气.
请回答:
(1)有机化合物A中碳原子与氢原子的个数比是 , A的结构简式为 .
(2)化合物A在一定条件下脱水可生成B,B可加聚合成包装塑料.A转化为B的化学反应方程式为 .
(3)化合物A可在一定条件下通过粮食制得,由粮食制得的A在一定温度下密闭储存,由于发生一系列的化学变化而变得有酯香味.在这一系列变化过程中,最后一步化学变化的化学方程式为 , 反应类型为 .
(4)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27oC)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,制备反应方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
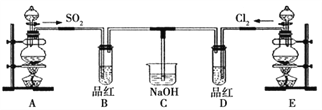
(1)实验室用装置A制备SO2。从物质类别看,SO2属于________(填“酸性”、“两性”或“碱性”)氧化物;
(2)实验室用装置E制备Cl2,写出该反应的离子方程式:___________________________。当有0.2 mol电子转移时,产生氯气的体积(标准状况)是________,氧化剂与还原剂的物质的量之比是________。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________________,D:________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1︰1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)____________________________。
(5)有人预测SO2能使酸性高锰酸钾溶液褪色,你认为该预测是否合理?________(填“合理”或“不合理”),理由是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是氯碱工业的主要产品之一,常作强氧化剂,可与有机物和无机物进行反应生成多种氯化物。某兴趣小组在实验室中对以下反应进行了探究。回答下列问题:
Ⅰ、三氯化硼(BCl3)的制备,已知:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃; ②2B+6HCl ![]() 2BCl3↑+3H2↑。
2BCl3↑+3H2↑。

(1)按气流方向连接各装置的接口,顺序为a→( )→( )→( )→( )→( )→( )→f→g→h。_________
(2)装置D的作用是_____________;实验中若不用装置C,可能产生的危险是____________。
(3)BCl3遇水发生水解观察到大量的白雾,生成两种酸,其反应的化学方程式为:___________。
Ⅱ、SO2与漂粉精溶液的反应
操作 | 现象 |
取4g 漂粉精固体,加入100mL 水,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
| 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(4)pH试纸颜色的变化说明漂粉精溶液具有的性质是_____________________________。
(5)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl- 发生反应。该反应的离子方程式为________________________。
(6)用离子方程式解释现象3中黄绿色褪去的原因_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中的氯化镁是镁的重要来源之一。下列从海水中提取镁涉及的化学方程式中,不正确的是
A. 制石灰乳:CaO + H2O === Ca(OH)2
B. 制氢氧化镁:MgCl2 + Ca(OH)2 === Mg(OH)2↓+ CaCl2
C. 制氯化镁:Mg(OH)2 +2HCl === MgCl2 + 2H2O
D. 制金属镁,在氯化镁溶液中加钠:2Na + MgCl2 === 2NaCl + Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某同学用下图所示的装置做了有关氨气的性质实验。
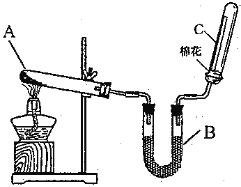
(1)写出A处氯化铵固体与熟石灰共热反应的化学方程式:_____________________________。
(2)B中盛放的是碱石灰,其作用是_____________________________。
(3)氨气极易溶于水,在氨水中滴加酚酞,现象是_________________________________。
(4)检验氨气的方法是___________________________________________________________。
Ⅱ.乙烯是一种重要的有机化工原料。在一定条件下乙烯可发生如下转化:
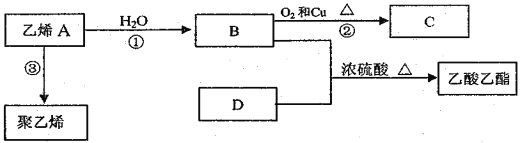
(1)乙烯的结构简式是_______________,D的分子式是_______________。
(2)B中含氧官能团的名称是_____________,③的反应类型是______________。
(3)写出反应②的化学方程式: ________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于强弱电解质,下列说法正确的是
A. 液态HC1和液态H2O中都不存在离子
B. 室温下,硫酸溶液的pH—定小于醋酸溶液
C. 二种弱电解质在一定条件下可以相互反应生成强电解质
D. NaX在水中的电离方程式为NaX=Na++X-,因此HX是一种强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:
C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热△H为( )
A.3.8×104kJmol﹣1
B.﹣3.8×104kJmol﹣1
C.3.4×104kJmol﹣1
D.﹣3.4×104kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,导致所配溶液浓度偏低的原因可能是
A.容量瓶中原有少量的蒸馏水B.溶解后没有冷却就转移到容量瓶中
C.移液时,不慎将液体流到瓶外D.定容时,俯视观察刻度线和液面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com