
一定温度下,下列溶液中的粒子浓度关系式正确的是
A.0.1mol·L-1的NaHS溶液中:c(OH-)=c(H+)+c(H2S)
B.往氯化铵溶液中加水 的值变大
的值变大
C.0.1mol·L-1的NaOH溶液与0.2mol·L的HA溶液等体积混合,所得溶液呈碱性:c(Na+)>c(HA)>c(A-)>c(OH-)>c(H+)
D.pH相等的①NH4Cl ②NH4Al(SO4)2 ③NH4HSO4溶液中,c(NH4+)大小顺序:①>②>③
科目:高中化学 来源:2016-2017学年吉林省高一上期初化学卷(解析版) 题型:选择题
下列溶液中的氯离子浓度与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是
A.75 mL 2 mol·L-1的CaCl2 B.75 mL 1 mol·L-1的NH4Cl
C.150 mL 1 mol·L-1的NaCl D.150 mL 3 mol·L-1的KCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上第一次考试化学卷(解析版) 题型:选择题
实验室里需用480mL 0.1mol/L的硫酸铜溶液,配制时应选择的容量瓶的规格和需要称量的溶质的质量分别为
A.480mL容量瓶,7.68g硫酸铜 B.480mL容量瓶,12.0g胆矾
C.500mL容量瓶,12.5g硫酸铜 D.500mL容量瓶,12.5g胆矾
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
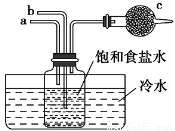
A.a通入CO2,然后b通入NH3,c中放碱石灰
B .b通入NH3,然后a通入CO2,c中放碱石灰
.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上第12次周测化学卷(解析版) 题型:填空题
已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是 (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序排列为 (用元素符号表示)。
(4)C的单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有 (填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为 ;B和E的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为acm,则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上第12次周测化学卷(解析版) 题型:选择题
分子式为C6H12O2的酯共有(不考虑立体异构)
A.18种 B.19种 C.20种 D.21种
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10月月考化学试卷(解析版) 题型:选择题
向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大下列对应关系正确的是( )
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:填空题
(1)有下列物质①Cu ②液氨 ③CH3COOH ④NaHCO3 ⑤H2O ⑥熔融NaCl ⑦NH3·H2O ⑧NH4Cl 属于弱电解质的是 (填序号)。
化学式 | NH3·H2O | HCN | CH3COOH | H2CO3 |
电离平衡常数(25℃) | Kb=1.77×10-5 | Ka=4.93×10-10 | Ka=1.76×10-9 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。上表中给出几种弱电解质的电离平衡常数,从中可以判断:在相同温度下,同浓度的三种酸溶液的导电能力由大到小的顺序为 。
(3)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液 b.Na2CO3溶液 c.CH3COONa溶液,三种溶液的pH由大到小的顺序为 。(填溶液前序号)
②浓度相同的NaCN溶液与CH3COOK溶液相比,c(Na+)—c(CN-) c(K+)-c(CH3COO-)。(填“>”“<”或“=”)
③将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈 性(填“酸”、“碱”或“中”),用离子方程式表示原因 。
④室温下,若将0.1mol·L-1盐酸滴入20ml0.1mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。b点所示溶液中的溶质是 。
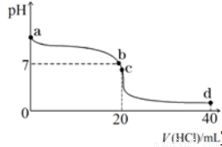
⑤NH4HCO3溶液呈 性(填“酸”、“碱”或“中”)。
(4)结合表中数据,向NaCN溶液中通入少量CO2,所发生反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学卷(解析版) 题型:选择题
在水中加等物质的量的Ag+、Pb2 +、Na +、 SO42 -、 NO3- 、 Cl-,该溶液放在用惰性电极做电极的电解槽中,通电片刻,则氧化产物与还原产物质量
-、 NO3- 、 Cl-,该溶液放在用惰性电极做电极的电解槽中,通电片刻,则氧化产物与还原产物质量 比为( )
比为( )
A.35.5:108 B. 16:207 C.8:1 D.108:35.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com