
| A.浓硝酸和浓硫酸都具有很强的腐蚀性、脱水性 |
| B.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 |
| C.稀硫酸和稀硝酸都具有氧化性 |
| D.硫酸和硝酸都是重要的化工原料 |
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| A.SO2使酸性KMnO4溶液褪色 | B.SO2使溴水褪色 |
| C.SO2使品红溶液褪色 | D.SO2使含酚酞的NaOH溶液褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.仅①和④ | B.仅①和③ | C.仅②和③ | D.仅②和④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
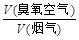 流量比为y,请通过计算列出y与x的关系式。
流量比为y,请通过计算列出y与x的关系式。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2能与碱反应,推测:非金属氧化物都能与碱反应 |
| B.金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭 |
| C.Fe3O4可表示为FeO·Fe2O3,推测:Pb3O4也可表示为PbO·Pb2O3 |
| D.F-Cl-Br-I的单质熔点依次升高,推测:N-P-As-Sb-Bi的单质熔点也依次升高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质硫在空气中燃烧可生成SO2 |
| B.SO2能使品红溶液褪色是因为它具漂白性,加热可恢复原本红色 |
| C.SO2和Cl2都具有漂白作用,所以将两种气体等物质的量同时作用于潮湿有色物,可增强漂白作用 |
| D.SO2能使加酚酞的NaOH溶液褪色是因为它能与NaOH反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
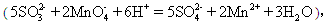 消耗KMnO4溶液b mL。
消耗KMnO4溶液b mL。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com