
�״���һ�ֻ���ԭ�ϣ���ҵ�Ϻϳɼ״��ķ�Ӧ��
CO(g)��2H2(g)![]() CH3OH(g) ��H= -90.8kJ��mol-1��
CH3OH(g) ��H= -90.8kJ��mol-1��
�����¶ȡ��ݻ���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molCO .2molH2 | 1mol CH3OH | 2molCO��4molH2 |
| CH3OH��Ũ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�Q1 kJ | ����Q2 kJ | �ų�Q3 kJ |
| ƽ�ⳣ�� | K1 | K2 | K3 |
| ��Ӧ��ת���� | �� 1 | �� 2 | �� 3 |
�٣�������ѹǿP��2P����2P����P����ϵ��
�ڣ��仯��������ֵQ�У� Q1 ��Q2�ĺ���
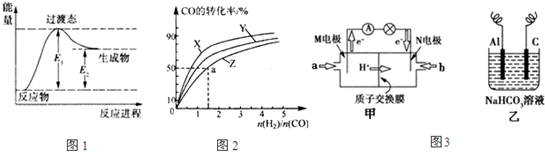
�ۣ�����ƽ��ʱ�״��İٷֺ���(������)���¶�(������)�ı仯���ߣ�
Ҫ��ѹǿ��ͬ����������(���p1��p2����p1<p2)��
�ܣ���һ���¶Ⱥ�ѹǿ�£�CO��H2���ϳɶ����ѷ�ӦΪ��
3H2��g��+3CO��g��![]() CH3OCH3��g��+CO2��g����ͼΪ��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء�����ԭ��ʾ��ͼ��a�缫�ķ�ӦʽΪ
CH3OCH3��g��+CO2��g����ͼΪ��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء�����ԭ��ʾ��ͼ��a�缫�ķ�ӦʽΪ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 �״�����Ҫ�Ļ���ԭ�ϣ����ճ����������Ź㷺��Ӧ�ã�
�״�����Ҫ�Ļ���ԭ�ϣ����ճ����������Ź㷺��Ӧ�ã� CH3OH��g����H1
CH3OH��g����H1 CH3OH��g��+H2O��g����H2
CH3OH��g��+H2O��g����H2| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molCO.2molH2 | 1mol CH3OH | 2molCO��4molH2 |
| CH3OH��Ũ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�Q1 kJ | ����Q2 kJ | �ų�Q3 kJ |
| ƽ�ⳣ�� | K1 | K2 | K3 |
| ��Ӧ��ת���� | �� 1 | �� 2 | �� 3 |
 Ϊ��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء�����ԭ��ʾ��ͼ��a�缫�ķ�ӦʽΪ
Ϊ��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء�����ԭ��ʾ��ͼ��a�缫�ķ�ӦʽΪ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ������ʡ��«��һ�߸߶���ѧ�ڵ�һ���¿���ѧ�Ծ����������� ���ͣ������
�״���һ�ֻ���ԭ�ϣ���ҵ�Ϻϳɼ״��ķ�Ӧ��
CO(g)��2H2(g) CH3OH(g) ��H= -90.8kJ��mol-1��
CH3OH(g) ��H= -90.8kJ��mol-1��
�����¶ȡ��ݻ���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molCO .2molH2 | 1mol CH3OH | 2molCO��4molH2 |
| CH3OH��Ũ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�Q1 kJ | ����Q2 kJ | �ų�Q3 kJ |
| ƽ�ⳣ�� | K1 | K2 | K3 |
| ��Ӧ��ת���� | �� 1 | �� 2 | �� 3 |
 CH3OCH3��g��+CO2��g����ͼΪ��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء�����ԭ��ʾ��ͼ��a�缫�ķ�ӦʽΪ
CH3OCH3��g��+CO2��g����ͼΪ��ɫ��Դ��ֱ�Ӷ�����ȼ�ϵ�ء�����ԭ��ʾ��ͼ��a�缫�ķ�ӦʽΪ �鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com