
下列有关实验的说法正确的是 。
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)〈Ksp(CuS)
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
氯元素的相对原子质量为35.5,氯只有35Cl和37Cl两种稳定同位素,在氯气中35Cl和37Cl的原子个数比为3∶1,则相对分子质量为70,72,74的氯气分子数之比可能是( )
A.5∶3∶2 B.5∶2∶2 C.5∶2∶1 D.9∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A.溶液中导电粒子的数目增加,导电性增强 B.醋酸的电离程度增大,[H+]减小
C.再加入10mL pH=11 NaOH溶液,混合液pH=7 D.溶液中由水电离出的[H+]=1×10-11 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:Zn+2OH-=Zn(OH)2 +2e-; Ag2O +H2O +2e- =2Ag +2OH-。下列说法错误的是
A.溶液中OH-向正极移动 B.锌发生氧化反应
C.氧化银是正极 D.在电池放电过程中,电解质溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
1)25℃时,浓度为0.1 mol·L-1的6种溶液:①HCl, ②CH3OOH, ③Ba(OH)2,④Na 2CO3,⑤KCl,⑥NH4Cl溶液pH由小到大的顺序为__________________(填写编号)。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh= mol ·L-1(保留到小数点后一位)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈 (填“酸性”,“中性”或“碱性”) ,请写出溶液中离子浓度间的一个等式: 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH=7,
则溶液中c(CH3COO-) + c(CH3COOH)= ,m与n的大小关系是m n(填“ >”“=”或“<” )。
(5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,则NH3·H2O的电离常数Ka= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
滴加新制氯水后,下列各组离子可能大量存在的是
A.Fe3+、Cl-、NO3- B.Na+、HCO3-、SO42-
C.Ag+、NH4+、NO3- D.Na+、SO32-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的工业制备原理的方程式书写正确的是
A.乙醇:C6H12O6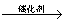 2CH3CH2OH + 2CO2↑
2CH3CH2OH + 2CO2↑
|
 CH2=CH2↑+ H2O
CH2=CH2↑+ H2O C.盐酸:NaCl + H2SO4 NaHSO4 + HCl↑
NaHSO4 + HCl↑
D.纯碱:2NaCl + 2NH3 + CO2 + H2O → Na2CO3↓+ 2NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
对已达化学平衡的下列反应 2X(g)+Y(g) 2Z(g)减小压强时,对反应
2Z(g)减小压强时,对反应
产生的影响是
A. .逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B. .逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C. .正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com