
·ÖĪö ½įŗĻc=$\frac{n}{V}$¼°²»µ±²Ł×÷¶Ōn”¢VµÄÓ°ĻģÅŠ¶Ļ¶ŌĪļÖŹµÄĮæÅØ¶ČµÄÓ°Ļģ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©½«ĒāŃõ»ÆÄĘ¹ĢĢå·ÅŌŚĀĖÖ½ÉĻ½ųŠŠ³ĘĮ棬NaOHµÄÖŹĮæĘ«Š”£¬nĘ«Š”£¬ÓÉc=$\frac{n}{V}$æÉÖŖ£¬ÅضČĘ«µĶ£¬¹Ź“š°øĪŖ£ŗĘ«µĶ£»
£Ø2£©Ī“½«Ļ“µÓŅŗ¼ÓČėČŻĮæĘ棬nĘ«Š”£¬ÓÉc=$\frac{n}{V}$æÉÖŖ£¬ÅضČĘ«µĶ£¬¹Ź“š°øĪŖ£ŗĘ«µĶ£»
£Ø3£©¶ØČŻŹ±ŃöŹÓæĢ¶ČĻߣ¬VĘ«“ó£¬ÓÉc=$\frac{n}{V}$æÉÖŖ£¬ÅضČĘ«µĶ£¬¹Ź“š°øĪŖ£ŗĘ«µĶ£»
£Ø4£©Ņ”ŌČŗó·¢ĻÖ°¼ŅŗĆęĻĀ½µ£¬ÓÖ¼ÓÕōĮóĖ®ÖĮæĢ¶ČĻߣ¬VĘ«“ó£¬ÓÉc=$\frac{n}{V}$æÉÖŖ£¬ÅضČĘ«µĶ£¬¹Ź“š°øĪŖ£ŗĘ«µĶ£»
£Ø5£©ÅäÖĘĒ°ČŻĮæĘæÓĆĖ®Ļ“µÓŗóĪ“½ųŠŠøÉŌļ“¦Ąķ£¬¶ŌŹµŃéĪŽÓ°Ļģ£¬¹Ź“š°øĪŖ£ŗĪŽÓ°Ļģ£»
£Ø6£©ĒāŃõ»ÆÄĘČÜŅŗĪ“ĄäČ“ÖĮŹŅĪĀ¾Ķ×ŖŅʵ½ČŻ×īĘ棬VĘ«Š”£¬ÓÉc=$\frac{n}{V}$æÉÖŖ£¬ÅضČĘ«øߣ¬¹Ź“š°øĪŖ£ŗĘ«øߣ®
µćĘĄ ±¾Ģāæ¼²éÅäÖĘŅ»¶ØÅØ¶ČµÄČÜŅŗ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄĮ攢Ģå»ż”¢ÅØ¶ČµÄ¹ŲĻµĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬עŅā½įŗĻ¹«Ź½¼°²Ł×÷·ÖĪöĪó²ī£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH=Na++OH- | B£® | Na2SO4=2Na++SO4-2 | ||
| C£® | H2SO4=H2++SO42- | D£® | Ca£ØNO3£©2=Ca2++2£ØNO3£©2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ŌŖĖŲXĪ»ÓŚµŚĖÄÖÜĘŚ£¬Ę仳Ģ¬Ō×ÓµÄÄŚ²ć¹ģµĄČ«²æÅÅĀśµē×Ó£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖ2£»ŌŖĖŲY»łĢ¬Ō×ÓµÄ3p¹ģµĄÉĻÓŠ4øöµē×Ó£®XÓėYŠĪ³ÉµÄ»ÆŗĻĪļµÄ¾§°ūČēĶ¼ĖłŹ¾£¬ĻĀĮŠ¹ŲÓŚøĆ¾§ĢåµÄĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŌŖĖŲXĪ»ÓŚµŚĖÄÖÜĘŚ£¬Ę仳Ģ¬Ō×ÓµÄÄŚ²ć¹ģµĄČ«²æÅÅĀśµē×Ó£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖ2£»ŌŖĖŲY»łĢ¬Ō×ÓµÄ3p¹ģµĄÉĻÓŠ4øöµē×Ó£®XÓėYŠĪ³ÉµÄ»ÆŗĻĪļµÄ¾§°ūČēĶ¼ĖłŹ¾£¬ĻĀĮŠ¹ŲÓŚøĆ¾§ĢåµÄĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | 1øö¾§°ūÖŠĄė×ÓµÄ×ÜŹżĪŖ18 | |
| B£® | X2+Ąė×ÓµÄÅäĪ»ŹżĪŖ8£¬Y2-Ąė×ÓµÄÅäĪ»ŹżĪŖ4 | |
| C£® | ÓėĆæøöX2+¾ąĄė×ī½üµÄX2+¹²ÓŠ12øö | |
| D£® | øĆ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖCaS |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
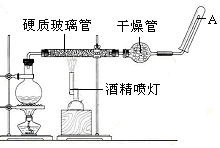 ŌŚ³£ĪĀĻĀ£¬FeÓėĖ®²¢²»Ęš·“Ó¦£¬µ«ŌŚøßĪĀĻĀ£¬FeÓėĖ®ÕōĘųæÉ·¢Éś·“Ó¦ÓĆĻĀĮŠ×°ÖĆ£¬ŌŚÓ²ÖŹ²£Į§¹ÜÖŠ·ÅČė»¹ŌĢś·ŪŗĶŹÆĆŽČŽµÄ»ģŗĻĪļ£¬¼ÓČČ£¬²¢ĶØČėĖ®ÕōĘų£¬¾ĶæÉŅŌĶź³ÉøßĪĀĻĀ”°FeÓėĖ®ÕōĘųµÄ·“Ó¦ŹµŃé”±£®
ŌŚ³£ĪĀĻĀ£¬FeÓėĖ®²¢²»Ęš·“Ó¦£¬µ«ŌŚøßĪĀĻĀ£¬FeÓėĖ®ÕōĘųæÉ·¢Éś·“Ó¦ÓĆĻĀĮŠ×°ÖĆ£¬ŌŚÓ²ÖŹ²£Į§¹ÜÖŠ·ÅČė»¹ŌĢś·ŪŗĶŹÆĆŽČŽµÄ»ģŗĻĪļ£¬¼ÓČČ£¬²¢ĶØČėĖ®ÕōĘų£¬¾ĶæÉŅŌĶź³ÉøßĪĀĻĀ”°FeÓėĖ®ÕōĘųµÄ·“Ó¦ŹµŃé”±£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬1L 0.1mol/L HClČÜŅŗÖŠŗ¬ĒāŌ×ÓŹżŹĒ0.1NA | |
| B£® | ±ź×¼×“æöĻĀ£¬2.24LÓÉCO2ŗĶO2×é³ÉµÄ»ģŗĻĘųĢåÖŠŗ¬Ńõ·Ö×ÓŹżŹĒ0.1NA | |
| C£® | 10gĢ¼ĖįøĘÓė×ćĮæµÄĻ”ŃĪĖį³ä·Ö·“Ó¦ĻūŗĵÄĒāĄė×ÓŹżĪŖ0.1NA | |
| D£® | ±ź×¼×“æöĻĀ£¬11.2L COŗĶ NO»ģŗĻĘųĢåÖŠÓė11.2LN2ÖŠ·Ö×ÓŹż¾łĪŖ0.5NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Į½ÖÖĘųĢåµÄŃ¹ĒæĻąµČ | B£® | O2ŗĶO3µÄŌ×ÓøöŹżĻąµČ | ||
| C£® | Į½ÖÖĘųĢåµÄŃõ»ÆÄÜĮ¦ĻąĶ¬ | D£® | Į½ÖÖĘųĢåµÄ·Ö×ÓŹżÄæĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | 8 ÖÖ | B£® | 7ÖÖ | C£® | 6ÖÖ | D£® | 5ÖÖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com