
 实验探究气体的体积与物质的量的关系:
实验探究气体的体积与物质的量的关系:分析 (1)分析装置图可知与电源正极相连的电极为电解池阳极,与电源负极相连的电极为电解池阴极,水中氢氧根离子移向阳极失电子生成氧气,氢离子得到电子生成氢气,电池反应为电解水;
(2)气体物质的量之比等于气体体积比,结合化学方程式定量关系计算;
解答 解:(1)分析装置图可知与电源正极相连的电极为电解池阳极,与电源负极相连的电极为电解池阴极,水中氢氧根离子移向阳极失电子生成氧气,氢离子得到电子生成氢气,电池反应为电解水,2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,二者的体积比是2:1,
故答案为:H2,O2,2:1;
(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,
36 4 32
1.8g 0.2g 1.6g
生成氢气物质的量=$\frac{0.2g}{2g/mol}$=0.1mol,
生成氧气物质的量=$\frac{1.6g}{32g/mol}$=0.05mol,
二者物质的量之比0.1:0.05=2:1
故答案为:0.2,0.1,1.6,0.05,2:1;
点评 本题考查了电解原理的理解应用,电极名称和电极反应分析,化学方程式定量计算是解题关键,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 稀盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
| A. | 1.00mol•L-1 | B. | 0.50mol•L-1 | C. | 1.50mol•L-1 | D. | 2.00mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
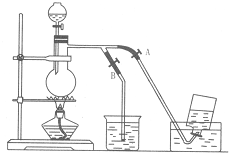 如图表示在没有通风橱收纯净的氯气时设计的装置,图中A、B是可控制的弹簧铁夹.
如图表示在没有通风橱收纯净的氯气时设计的装置,图中A、B是可控制的弹簧铁夹. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c、d、f之比可能为16:1:3 | |
| B. | 一定有a=2e,b=e | |
| C. | 若n(KClO):n(KClO3)=1:1,则a、b、c、d、e、f依次为8:4:6:1:4:1 | |
| D. | 若将该方程式拆开写成两个“半反应”,其中一定有Cl2-2e-=2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2+Ca(OH)2═CaCl2+Mg(OH)2↓ | B. | Mg(OH)2+2HCl═MgCl2+2H2O | ||
| C. | Mg(OH)2+H2SO4═MgSO4+2H2O | D. | MgCl2$\frac{\underline{\;通电\;}}{熔融}$Mg+Cl2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com