
下列过程或现象与盐类水解无关的是
A.纯碱溶液去油污 B.稀醋酸溶液加热时其pH 减小
C.小苏打溶液与AlCl3溶液混合产生气体和沉淀 D.浓的硫化钠溶液有臭味
B
【解析】
试题分析:A.纯碱Na2CO3是强碱弱酸盐,水解使溶液显碱性。而油污属于酯,在碱性条件下水解得到高级脂肪酸钠与甘油等容易溶解于水的物质。因此纯碱溶液能够去油污。错误。B.醋酸是弱酸,,电离需要吸收热量。升高温度,促进醋酸的电离。使溶液的酸性增强,其pH 减小。但是这与盐类水解无关。正确。C.小苏打NaHCO3是强碱弱酸盐,水解使溶液显碱性;而AlCl3是强酸弱碱盐,水解使溶液酸性,二者混合,发生双水解反应产生CO2气体和Al(OH)3沉淀.与盐的水解有关。错误。D.浓的硫化钠是强碱弱酸盐,水解产生H2S。浓度大,水解产生H2S多,所以溶液会逸出H2S的臭鸡蛋的臭味。
考点:考查盐的水解在生活、生产中的应用的知识。


 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:推断题
某有机化合物A,分子式为C8H9Cl,其苯环上的一溴代物只有三种,该物质能发生下列一系列变化
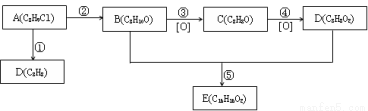
⑴反应②的条件 ,A的结构简式
⑵写出下列有关反应的化学方程式
A →D: ; B →C: ;
C →D: B+D →E:
⑶B的同分异构体中,写出苯环侧链上有二个取代基,能与金属钠反应产生H2、不能使FeCl3溶液显紫色的所有同分异构体的结构简式
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
在25℃时将pH=11 的NaOH 溶液与pH=3 的CH3COOH溶掖等体积混合后,下列关系式中正确的是
A.c (Na+)=c(CH3COO-)+c(CH3COOH)
B.c(H+)=c(CH3COO-)+c(OH一)
C.c (Na+) > c (CH3COO-)>c(OH-)>c(H+)
D.c (CH3COO-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
下面是关于中和滴定的实验叙述:取25.00 mL未知浓度的HCl溶液。在横线标明操作中,有错误的是
a.放入锥形瓶中,此瓶需事先用蒸馏水洗净。 b.并将该瓶用待测液润洗过。
c.加入几滴酚酞作指示剂。 d.取一支酸式滴定管,经蒸馏水洗净。
e.直接往其中注入标准NaOH溶液,进行滴定。
f.一旦发现溶液由无色变成粉红色,即停止滴定,记下数据。
A.d、e、f B.b、d、e、f C.b、d、e D.b、c、e、f
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省高三5月冲刺卷理综化学试卷(解析版) 题型:选择题
在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应如下:2A(g)+B(g) 2D(g) △H=-QKJ·mol-1。相关条件和数据见下表:
2D(g) △H=-QKJ·mol-1。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 800 | 800 | 850 |
达平衡时间/min | 40 | 10 | 30 |
c(D)平衡/mol·L-1 | 0.5 | 0.5 | 0.15 |
反应的能量变化/KJ | Q1 | Q2 | Q3 |
下列说法正确的是
A.可用压强或密度是否发生变化判断上述反应是否达到平衡
B.实验Ⅱ可能隐含的条件是使用催化剂,实验Ⅲ达平衡时υ(D)为0.01mol·L-1·min-1
C.由表中信息可知Q>O,并显有Q3<Q2=Q1=Q
D.实验Ⅰ达平衡后,恒温下再向容器中通入1molA和1molD,达平衡时c(D)为1.0mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:填空题
(12分)铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知铁
与冷的稀HNO3反应时,主要还原产物为NO气体;与热的稀HN03反应时,主要还原产物
为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀 HNO3的作用,请分析
下图,回答有关问题。
假设曲线的各段内只有一种还原产物。
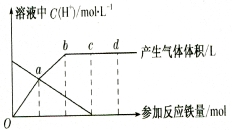
(1)0点到a点的还原产物是 ________ __ 。
(2)a点到b点的还原产物是__ __,其原因是 。
(3)试完成b点到c点的反应方程式:
口Fe+口HNO3——口Fe( NO3)3+口[ ]+口H20。
(4)反应过程中,到达 ________ 点时,HN03已完全反应。
(5)已知达到d点时反应结束,此时溶液中的主要阳离子是 。
(6)c点和d点参加反应的铁的物质的量之比是 ___________ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+ 。下列叙述不正确的是
A.氧化产物为Cl2
B.氧化剂与还原剂的物质的量之比为1∶2
C.若有3mol H2O生成,则反应中有2mol电子转移
D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省白城市高二上学期期末考试化学(B卷)试卷(解析版) 题型:选择题
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是
A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-===AlO2-+2H2O
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-===Cu2+
D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗铜电极32 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com