
����Ŀ����֪���ᡢ�������������Һ�д�������ƽ�⼰���Ӧ��ƽ�ⳣ��
CH3COOH![]() CH3COO-+H+K1=1.75��10-5��H1>0
CH3COO-+H+K1=1.75��10-5��H1>0
CH3COO-+H20![]() CH3COOH+OH-K2=5.71��10-10��H2>0
CH3COOH+OH-K2=5.71��10-10��H2>0
�����£���������������ʵ���Ũ�ȵĴ���ʹ�������Һ��ϣ�����������ȷ����
A. �¶Ȳ���,���ڻ����Һ�м�������NaOH���壬c(CH3COO-)��С
B. �Ի����Һ�����ȣ�K1����K2��С
C. ���ڻ����Һ��pHֵ�����ԣ����ʱ��Һ��c(Na+)>c(CH3COO-)
D. ��֪ˮ�����ӻ�ΪKw�������߹�ϵΪK1��K2=Kw
���𰸡�D
��������A. �¶Ȳ��䣬���ڻ����Һ�м�������NaOH���壬�ᷢ������кͷ�Ӧ��ʹ���ᷢ������ij̶���������c��CH3COO-������A������B. �Ի����Һ�����ȣ���ٽ���ĵ�����ε�ˮ��̶ȣ�����K1����K2Ҳ����B����C. ����Һ�д��ڵ���غ㣺c(H+)��c(Na+)=c(CH3COO-)+c(OH-) �����ڻ����Һ��PHֵ�����ԣ���c(H+)=c(OH-������ʱ��Һ��c(Na+)=c(CH3COO-)����C����D. ![]() ����D��ȷ������ѡD��
����D��ȷ������ѡD��


 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��ԭ��������������Ķ���������Ԫ�أ�����Ԫ��ԭ������֮��Ϊ35����C��ԭ��������A��2����A��B��C����Ԫ�صĵ������ʵ������¿ɷ�����ͼ��ʾ�ı仯������˵����ȷ����

A. �ס��ҡ����������ʵ�ˮ��Һ���Լ���
B. ���Ǽ����������������������
C. �ס��ҿ��ܶ���Ư���ԣ���Ư��ԭ����ͬ
D. ����ˮ��Һ�ڿ����г��ڷ��ã���Һ���ܻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����(SOCl2)��һ��Һ̬������е�Ϊ77�棬��ũҩ����ҩ��ҵ����;�㷺��SOCl2��ˮ���ҷ�Ӧ�����������ʹ����Ƽ�����ζ�����塣ʵ���Һϳ�SOCl2��ԭ��Ϊ��SO2+Cl2+SCl2 ![]() 2SOCl2������װ����ͼ��ʾ��
2SOCl2������װ����ͼ��ʾ��

�ش���������:
(1)����a ��������_______��װ��b ��������__________��
(2)ʵ������ȡSOCl2 ʱ����ѡ����������˳���Ǣޡ�______���٢ڡ�_____(ij���������Զ��ʹ��)��
(3)�����ܿڢ���_____(���ˮ����ˮ��)�ڣ���ʵ�����Ʊ����������ӷ���ʽΪ___________��
(4)��SOCl2 ��AlCl3��6H2O��ϼ��ȣ��ɵõ���ˮAlCl3���Խ���ԭ��________��
(5)��֪SCl2 �ķе�Ϊ50�档ʵ�������������ƿ�еĻ������뿪��ʵ�����������___������Ӧ�����ı�״���µ�Cl2�����Ϊ1120 mL�����õ�������SOCl26.76 g,��SOCl2 �IJ���Ϊ________(������λ��Ч����)��
(6)��֪:SOCl2 +4NaOH= Na2SO3+2NaCl +2H2O������Ƽ�ʵ��(��ѡ�Լ�:ϡ���ᡢϡ���ᡢ�Ȼ�����Һ�����ᱵ��Һ����������Һ��Ʒ����Һ) ����֤�Ȼ�������NaOH ��Һ��Ӧ�����Һ�д���Cl-__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
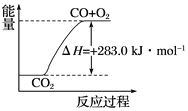
�� CO(g)�� ![]() O2(g)=CO2(g)����H�� ��283.0 kJ��mol��1
O2(g)=CO2(g)����H�� ��283.0 kJ��mol��1
�� H2(g)�� ![]() O2(g)=H2O(g)����H�� ��241.8 kJ��mol��1
O2(g)=H2O(g)����H�� ��241.8 kJ��mol��1
����˵����ȷ����( )
A. 1mol H-H����0.5mol O=O���ļ���֮�ʹ���2mol H-O ���ļ����ܺ�
B. �ɢٿ�֪��1 mol CO(g)�� ![]() mol O2(g)��Ӧ���� 1 mol CO2(g)���ų�283.0 kJ������
mol O2(g)��Ӧ���� 1 mol CO2(g)���ų�283.0 kJ������
C. ������ͼ��ʾ 2CO2(g)=2CO(g)��O2(g) ��Ӧ�����е������仯��ϵ
D. �ֽ�1 mol H2O(g)���䷴Ӧ��Ϊ��241.8 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��������װ����ȡ�ռ����������������о������ʡ���ش��������⡣

��1��װ�ü�������A��������________������Ӧװ����Һ��_______ ����װ���з�����Ӧ�����ӷ���ʽΪ_____________ ����ȡ�ռ�����������װ�ýӿ�����˳����a�� ����g(����������_________��
��2���Ʊ���Ӧ��������Ũ���½���ֹͣ��Ϊ�ⶨ��Ӧ����Һ�������Ũ�ȣ�̽��С��ͬѧ�������ʵ�鷽����
I������������AgNO3��Һ��Ӧ���������ɵ�AgCl������
������������к͵ζ����ⶨ��
��������֪��CaCO3����������Ӧ������ʣ���CaCO3������
�̶����������жϺ�ʵ�飺
���ж�I���������У�������__________________��
�ڽ��Т�ʵ�飺ȷ��ȡ������Һϡ��һ����������Ϊ������
a.��ȡ����20.00mL����ƿ�У�����ƿ�д�������ˮ����ʵ�����Ƿ���Ӱ�죿_____��ǡ��� ������0.10 molL-1NaOH����Һ�ζ�������NaOH����Һ�������ͼ��ʾ �������Ϊ _____mL.

b��ƽ�еζ�����ʵ����
���жϢ���ʵ����___________���ƫ����ƫС����ȷ������[��֪��Ksp��CaCO3����2.8��10-9��Ksp��MnCO3����2.3��10-11
��3�� ijͬѧ��Ϊ��������ȱ��β������װ�ã���������ķ����л�����װ�ò�ע���Լ�____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧԭ���ڹ�ҵ�����о���ʮ����Ҫ�����塣
��1����ҵ����������NH3(g)��CO2(g)��������Ӧ�������أ�������Ӧ�������仯ʾ��ͼ���£�
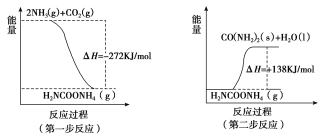
��NH3(g)��CO2(g)��Ӧ�������ص��Ȼ�ѧ����ʽΪ___________________________��
��2����֪��ӦFe(s)��CO2(g) ![]() FeO(s)��CO(g)����H��a kJ��mol��1������ڲ�ͬ�¶��£��÷�Ӧ��ƽ�ⳣ��K���¶ȵı仯���£�
FeO(s)��CO(g)����H��a kJ��mol��1������ڲ�ͬ�¶��£��÷�Ӧ��ƽ�ⳣ��K���¶ȵı仯���£�
�¶�(��) | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ��K�ı���ʽΪ____________��a________0(�>������<������)����500 �� 2 L�ܱ������н��з�Ӧ��Fe��CO2����ʼ����Ϊ4 mol����5 min��ﵽƽ��ʱCO2��ת����Ϊ________������CO��ƽ������v(CO)Ϊ_______________��
��700 �淴Ӧ�ﵽƽ���Ҫʹ��Ӧ����������ƽ�������ƶ��� �ɲ�ȡ�Ĵ�ʩ�� ___________��
��3������CO��H2��ֱ�Ӻϳɼ״�����ͼ���ɡ��״�-�������γɵ���ɫȼ�ϵ�صĹ���ԭ��ʾ��ͼ��д����ʯīΪ�缫�ĵ�ع���ʱ�����ĵ缫��Ӧʽ_____________________�����øõ�ص��1L 0��5mol/L��CuSO4��Һ��������560mLO2����״���£�ʱ��������Һ��pH��_________����Һ���ǰ������ı仯���Բ��ƣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�� ______mol CO2�к�����ԭ������1.806��1024��H2O���Ӻ��е���ԭ������ͬ��
��2��0.4 mol SiH4����������ԭ������_________g HCl����������ԭ������ȡ�
��3����״���µļ����һ����̼�Ļ������8.96 L��������Ϊ7.60 g�����������м�������Ϊ______��һ����̼������Ϊ_________��
��4�������ʵ���O2�ͳ���(O3)��������֮��Ϊ____����O2��O3������ȣ�����ԭ����֮��Ϊ__________��
��5��200������MgCl2��KCl��Na2SO4�������ʵĻ��Һ�У���֪���к�Cl��1.5 mol��K����Na����1.5 mol��Mg2��Ϊ0.5 mol����SO42-�����ʵ���Ũ��Ϊ__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com