
 (1)燃料电池是一种高效、环境友好的发电装置.氢氧燃料电池已用于航天飞机.以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为2H2+4OH--4e-═4H2O,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将减小(填“增大”“减小”或“不变”).
(1)燃料电池是一种高效、环境友好的发电装置.氢氧燃料电池已用于航天飞机.以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为2H2+4OH--4e-═4H2O,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将减小(填“增大”“减小”或“不变”).分析 (1)通入氢气的一极为电池的负极,发生氧化反应,生成水;反应生成水,溶液的体积增大;
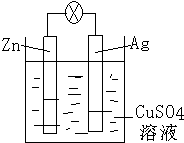
(2)该原电池中,Zn易失电子发生氧化反应而作负极,Ag作正极,负极上电极反应式为Zn-2e-=Zn2+,正极上电极反应式为Cu2++2e-=Cu,据此分析解答.
解答 解:(1)通入氢气的一极为电池的负极,氢气失电子发生氧化反应,生成水,则负极的电极方程式为2H2+4OH--4e-═4H2O;供电时的总反应为2H2+O2═2H2O,反应生成水溶液的体积增大,则c(OH-)将减小;
故答案为:2H2+4OH--4e-═4H2O;减小;
(2)锌易失电子发生氧化反应而作负极,电极反应式为Zn-2e-=Zn2+,所以锌片上看到的现象是金属逐渐溶解,总的电极反应式为:Zn+Cu2+=Zn2++Cu,故答案为:负;氧化;Zn-2e-=Zn2+;Zn+Cu2+=Zn2++Cu.
点评 本题考查原电池,为高频考点,把握电极的判断、电极反应的书写为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 大于2amol•L-1 | B. | 等于2amol•L-1 | C. | 小于2amol•L-1 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 +NaOH→
+NaOH→ +
+
 +HCl→
+HCl→

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验试剂及用量 | 溶液温度 | |||
| t1 | t2 | |||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ |
| ③ | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 24.5℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用装置①量取15.00mL的NaOH溶液 | |
| B. | 用装置②制备Cl2 | |
| C. | 用装置③陶瓷坩埚高温煅烧CaCO3固体 | |
| D. | 关闭活塞a,从b处加水,以检查装置④的气密性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 物质 | 正丁醇 | 正溴丁烷 |
| 沸点/℃ | 117.2 | 101.6 |
| 熔点/℃ | -89.12 | -112.4 |
| 密度/g•cm-3 | 0.8098 | 1.2758 |
| 溶解性 | 微溶于水,溶于浓硫酸 | 不溶于水和浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯通入酸性高锰酸钾溶液中 | B. | 乙烯通入溴水中 | ||
| C. | 苯与液溴在FeBr3催化下反应 | D. | 甲烷与氯气在一定条件下反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com