
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HC1O | H2CO3 |
| KSp 或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10 -5 | Ka=3.0×10-8 | Ka1=4.1×10一7 Ka2=5.6×10-11 |
| A. | 相同浓度CH3COONa和Na2CO3的混合液中,各离子浓度的关系有:c(Na+)>c(CO32- )>c(CH3COO- ) | |
| B. | 向0.1 mol•L-1 CH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时 c(CH3COOH):c(CH3COO-)=9:5 | |
| C. | 少量碳酸氢钠固体加入到新制的氯水中,c(HC1O)增大 | |
| D. | 向浓度均为1×10-3 mol•L-1的KC1和K2CrO4混合液中滴加1×10-3 mol•L-1 的AgNO3溶液,CrO42-先形成沉淀 |
分析 A.CH3COOH的Ka大于H2CO3的Ka2,可知同浓度时碳酸根离子水解程度大;
B.c(CH3COOH):c(CH3COO-)=c(H+):Ka;
C.少量碳酸氢钠固体加入到新制的氯水中,结合Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3)可知,氯气与水的反应正向移动;
D.由c(Ag+)=$\sqrt{Ksp(AgCl)}$、c(Ag+)=$\root{3}{4×Ksp(A{g}_{2}Cr{O}_{4})}$可知,AgCl的溶解度小.
解答 解:A.CH3COOH的Ka大于H2CO3的Ka2,可知同浓度时碳酸根离子水解程度大,则c(CO32- )<c(CH3COO- ),故A错误;
B.c(CH3COOH):c(CH3COO-)=c(H+):Ka=10-5:1.8×10 -5=5:9,故B错误;
C.少量碳酸氢钠固体加入到新制的氯水中,结合Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3)可知,碳酸氢根离子与氢离子反应,氯气与水的反应正向移动,c(HC1O)增大,故C正确;
D.由c(Ag+)=$\sqrt{Ksp(AgCl)}$=1.34×10 -5、c(Ag+)=$\root{3}{4×Ksp(A{g}_{2}Cr{O}_{4})}$=2.0×10-4,可知,AgCl的溶解度小,则Cl-先形成沉淀,故D错误;
故选C.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握离子浓度、Ksp的关系、盐类水解、平衡移动为解答的关键,侧重分析与计算能力的考查,注意表格中数据的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
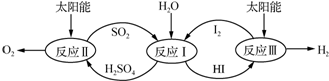
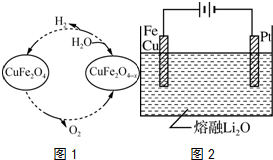
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
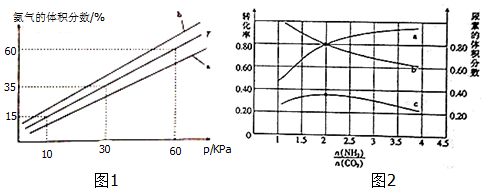
| 温度/K | 298 | 398 | 498 | … |
| 平衡常数(K) | 4.1×105 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
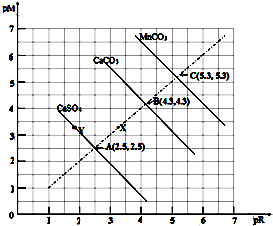
| A. | MnCO3在常温下的Ksp=2.5 x10-11(已知100.4=2.5) | |
| B. | 三种物质在常温下的溶解度大小顺序为MnCO3>CaCO3>CaSO4 | |
| C. | 处于Y点的CaSO4溶液中c(Ca2+)>c(SO42-) | |
| D. | Ca2+、CO32-浓度为X点的溶液可通过蒸发溶剂变为B点的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强/MPa C% 速度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
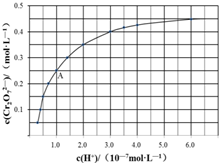 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com