
下列事实不能用勒夏特利原理来解释的是( )
|
| A. | 用排饱和食盐水的方法收集氯气 |
|
| B. | 合成氨工业选择高温 |
|
| C. | 增大压强,有利于SO2和O2反应生成SO3 |
|
| D. | 在Fe3++3SCN ﹣⇌Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
| 化学平衡移动原理. | |
| 专题: | 化学平衡专题. |
| 分析: | 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用. |
| 解答: | 解:A.实验室可用排饱和食盐水的方法收集氯气,氯气和水的反应是可逆反应,饱和氯化钠溶液中氯离子浓度大,化学平衡逆向进行,减小氯气溶解度,能用勒沙特列原理解释,故A不选; B.合成 NH3的反应为放热反应,升高温度平衡向逆反应方向移动,但升高温度为加快反应速率,与平衡移动无关,故B选; C.SO2和O2反应生成SO3,是气体体积缩小的反应,增大压强,有利于平衡正向移动,故C不选; D.增加KSCN的浓度,有利于平衡向正反应方向移动,Fe(SCN)3浓度增大,体系颜色变深,故D不选. 故选B. |
| 点评: | 本题考查了勒夏特列原理的使用条件,难度不大,注意把握影响平衡移动的因素以及使用勒夏特列原理的前提. |


科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.硫酸铝溶液中加入过量氨水
Al3++3OH-====Al(OH)3↓
B.碳酸钠溶液中加入澄清石灰水
Ca(OH)2+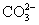 ====CaCO3↓+2OH-
====CaCO3↓+2OH-
C.冷的氢氧化钠溶液中通入氯气
Cl2+2OH-====ClO-+Cl-+H2O
D.稀硫酸中加入铁粉
2Fe+6H+====2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
为了说明影响化学反应速率快慢的因素,甲、乙、丙、丁四位同学分别设计了如下A﹣D四个实验,你认为结论不正确的是( )
|
| A. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
|
| B. | 将表面积、质量都相同的镁条和铝条分别与同浓度的盐酸反应,前者速率大于后者 |
|
| C. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
|
| D. | 相同条件下等质量的块状和粉末状大理石分别与相同浓度的盐酸反应时,粉末状的反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下面有关丙烷、丙烯、丙炔说法中正确的是
A.如图,丙烷、丙烯、丙炔的结构分别表示为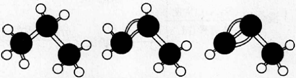
B.相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3 : 2 : 1
C.丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相同条件下密度逐渐增大
D.丙炔的碳原予空间结构呈线性排列
查看答案和解析>>
科目:高中化学 来源: 题型:
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示。加热聚丙烯废塑料得到的产物如下表所示:
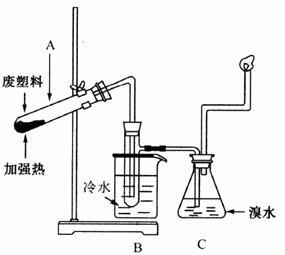
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 炭 |
| 质量分数(%) | 12 | 24 | 12 | 16[ | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
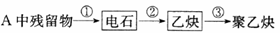
写出反应②、③的化学方程式_____________________。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有_________种。
(3) 锥形瓶C中观察到的现象是___________,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为___________。
(4) 写出C中逸出的气体在工业上的两种用途_________、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
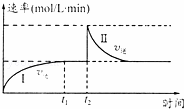
在一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)⇌2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图.下列说法正确的是( )
|
| A. | 0~t2时,v正>v逆 |
|
| B. | t2时刻改变的条件可能是加催化剂 |
|
| C. | Ⅰ、Ⅱ两过程达到反应限度时,A的体积分数Ⅰ=Ⅱ |
|
| D. | Ⅰ、Ⅱ两过程达到反应限度时,平衡常数I<Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
为解决能源危机,在汽油中掺入一定比例的乙醇(即“乙醇汽油”),以代替一部分汽油.乙醇在气缸中完全燃烧的热化学方程式为: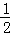 C2H5OH(l)+
C2H5OH(l)+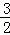 O2(g)=CO2(g)+
O2(g)=CO2(g)+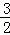 H2O(l)△H1=﹣683.4kJ/mol.下列说法正确的是( )
H2O(l)△H1=﹣683.4kJ/mol.下列说法正确的是( )
|
| A. | 该反应过程中,断裂化学键会放出热量 |
|
| B. | 该反应中,生成物的总能量大于反应物的总能量 |
|
| C. | 乙醇的燃烧热为683.4 kJ/mol |
|
| D. | 反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
pH相同的氨水、NaOH和Ba(OH)2溶液,分别用蒸馏水稀释到原来的X、Y、Z倍,稀释后三种溶液的pH仍然相同,则X、Y、Z的关系是( )
A.X=Y=Z B.X>Y=Z
C.X<Y=Z D.X=Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3分子的空间构型是三角锥形,而不是正三角形的平面结构,其充分的理由是( )
A. NH3分子是非极性分子
B.分子内3个N—H键的键长相等,键角相等
C. NH3分子内3个N—H键的键长相等,3个键角都等于107°18′
D. NH3分子内3个N—H键的键长相等,3个键角都等于120°
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com