
| װ�� | ���� | ���ۼ����� |
 | ��A�Թ��к�ɫ�������ܽ� ��A�Թ��Ϸ����ֺ���ɫ���� ��B�Թ��г��ְ�ɫ���� | a�������˵����ɫ�������� ��ԭ�ԣ� b���Թ�B�в�����ɫ�������ܷ�Ӧ�����ӷ���ʽΪ NO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+ |
���� ��1������ͭ��Ũ���ᷴӦ���ɶ�������������н��
��2������������Ϣ�м���ͭ���ӵķ����Ԣڽ��з�����Ȼ��ó���ȷ���ۣ�
��3��a������ɫ����Ϊ����������˵��ϡ���ᱻ��ԭ����һ����������ɫ������л�ԭ�ԣ�
b�����ݷ�Ӧ����ۿ�֪��ɫ������ϡ���ᷴӦ�����˶�������֤����ɫ�����к�����Ԫ�أ�������������������Ļ�������ܹ����Ȼ�����Ӧ�������ᱵ�������ݴ�д����Ӧ�����ӷ���ʽ��
��4��CuS����Һ�д��ڳ����ܽ�ƽ�⣬����ƽ���ƶ�������
��5�����ݵζ�ʵ�����ݼ���ʣ�����������ʵ������õ�������ͭ����ͭ��Ӧ�ĸ���������ʵ��������ݷ�Ӧ�����ӷ���ʽ��ʽ����õ���
��� �⣺��1��Cu��Ũ���ᷴӦ��������ͭ�����������ˮ����ӦΪCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+2SO2��+2H2O������������������SO2��
�ʴ�Ϊ��SO2��
��2������Һ�еμ�K4[Fe��CN��6]��Һ�����������ɫ������֤����Cu2+�����ݢڽ���ɫ��������ϡ�����У�һ��ʱ��μ�K4[Fe��CN��6]��Һ��δ�����ɫ������֪����ɫ������һ������CuO��
�ʴ�Ϊ����ɫ�����в�����CuO��
��3��a��A�Թ����Ϸ����ֺ���ɫ���壬˵����Ӧ����һ���������ɣ�֤���˺�ɫ������л�ԭ�ԣ��ڷ�Ӧ�б�������
�ʴ�Ϊ����ԭ��
b�����ݷ�Ӧ�����B�Թ��г��ְ�ɫ������֪����ɫ����Ϊ���ᱵ��˵����ɫ�����к�����Ԫ�أ�������Ӧ�����ӷ���ʽΪ��NO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+��
�ʴ�Ϊ��NO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+��
��4��CuS������ˮ����ˮ��Һ�л��к�������Cu�ܽ⣬��Һ�д��ڳ����ܽ�ƽ�⣬CuS��s��?Cu2+��aq��+S2-��aq�����ȵ�Ũ���ὫS2-������ʹS2-Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ⣻
�ʴ�Ϊ��CuS�����ܽ�ƽ��CuS��s��?Cu2+��aq��+S2-��aq�����ȵ�Ũ���ὫS2-������ʹS2-Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ⣻
��5�������ķ�ӦΪ��
8MnO4-+5Cu2S+44H+�T10Cu2++5SO2��+8Mn2++22H2O
6MnO4-+5CuS+28H+�T5Cu2++5SO2��+6Mn2++14H2O
MnO4-+5Fe2++8H+�TMn2++5Fe3++4H2O
��Cu2S��CuS�����ʵ����ֱ�Ϊx��y��
��Cu2S��CuS��Ӧ��ʣ��KMnO4�����ʵ�����0.035L��0.1mol/L��$\frac{1}{5}$=0.0007mol��
160x+96y=0.2
$\frac{8x}{5}$+$\frac{6y}{5}$=0.04��0.075-0.0007
���x=0.0005mol��
Cu2S������������$\frac{0.0005mol��160g/mol}{0.2g}$��100%=40%��
�ʴ�Ϊ��40%��
���� ���⿼����Ũ����Ļ�ѧ���ʡ�����ʵ�鷽������ƣ���Ŀ�Ѷ��еȣ������漰�������Դ�֪ʶ��϶࣬����������Ϣ�ǽ���ؼ�������������ѧ���ķ���������������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5 | B�� | 6 | C�� | 7 | D�� | 8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
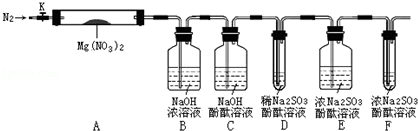
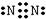 ��������У�ͨ��һ��ʱ��N2��Ŀ���DZ���Էֽ����O2�ļ���������ţ�
��������У�ͨ��һ��ʱ��N2��Ŀ���DZ���Էֽ����O2�ļ���������ţ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
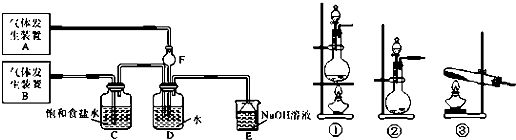
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬ�¶ȣ�2N2O4��g���T4NO2��g���ķ�Ӧ�Ⱥͻ�ѧƽ�ⳣ���ֱ�Ϊ-2��H��K2 | |
| B�� | �÷�Ӧ�ﵽƽ�����С�������ݻ���ƽ�����ƣ����������ɫ��dz | |
| C�� | ��Ͷ��2mol NO2��ͨ�����������������������1mol N2O4 | |
| D�� | ƽ��ʱһ����v����NO2��=2v����N2O4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ�еμ�Ba��OH��2��Һ��ǡ��ʹSO${\;}_{4}^{2-}$������ȫ2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4�� | |
| B�� | ����������������Һ��Al+2OH-+H2O�TAlO2-+H2�� | |
| C�� | �����Լ�ƿ���ռ���Һ��ʴ��SiO2+2Na++2OH-�TNa2SiO3��+H2O | |
| D�� | VO2+�����Ը��������Һ��Ӧ��5VO2++MnO${\;}_{4}^{-}$+H2O�T5VO${\;}_{2}^{+}$+Mn2++2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����γ��ȶ�����̬�⻯�� | B�� | ��ԭ���������6������ | ||
| C�� | ������������ˮ������ǿ�� | D�� | X�ǽ���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.21 mol | B�� | 0.25 mol | C�� | 0.3 mol | D�� | 0.35mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com