
(15分)某合作学习小组的同学拟用硼砂制取硼酸并测定硼酸样品的纯度。制备硼酸的实验流程如下:

(1)溶解硼砂时需要的玻璃仪器有:烧杯和 。
(2)用pH试纸测定溶液pH的操作方法为 。
(3)用盐酸酸化硼砂溶液生成硼酸的离子方程式为 。
(4)实验流程中缺少的步骤a、步骤b操作分别为 、 。
(5)硼酸酸性太弱不能用碱的标准溶液直接滴定,实验室常采用间接滴定法,其原理为:
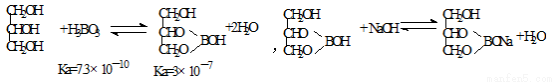
滴定步骤为:

①定到终点时溶液颜色变化是 。
②若滴定到终点时消耗NaOH标准溶液22.00mL,则本次滴定测得的硼酸样品中硼酸的质量分数为 (假定杂质不反应)。
③若滴定时滴定管尖嘴部分有气泡,滴定过程中消失,将导致测得的结果 (选填:“偏大”、“偏小”或“不变”)。
(1)玻璃棒(1分)
(2)用干燥洁净的玻璃棒蘸取待测溶液点在试纸中央,半分钟内与标准比色卡进行对照,判断溶液的pH(2分)
(3)B4O72-+2H++5H2O = 4H3BO3(2分)(4)过滤(2分)、洗涤(2分)
(5)①由无色变为浅红色(2分) ②90.93%(2分)③偏大(2分)
【解析】
试题分析:(1)溶解物质时一般是在烧杯中进行,为了加速物质的溶解,通常使用玻璃棒搅拌。所以硼砂时需要的玻璃仪器有:烧杯和玻璃棒;(2)用pH试纸测定溶液pH的操作方法为用干燥洁净的玻璃棒蘸取待测溶液点在试纸中央,半分钟内与标准比色卡进行对照,判断溶液的pH;(3)根据强酸制取弱酸的性质,盐酸与硼砂溶液发生反应生成硼酸的离子方程式为B4O72-+2H++5H2O = 4H3BO3;(4)实验流程中把晶体从溶液中分离出来的方法是过滤,洗涤晶体,所以缺少的步骤a、步骤b操作分别为过滤、洗涤;(5)①由于是用碱溶液滴定酸,指示剂酚酞在酸性溶液中,所以当达到滴定到终点时溶液颜色变化是溶液由无色变为浅红色,半分钟内不褪色,就证明达到了滴定终点;②若滴定到终点时消耗NaOH标准溶液22.00mL,n(NaOH)=0.2mol/L×2.2×10-3L=4.4×10-4mol/L,根据方程式中二者的物质的量的关系可知n(H3BO3)= 4.4×10-4mol/L,所以m(H3BO3)= 4.4×10-4mol/L×62g/mol=0.2728g,则本次滴定测得的硼酸样品中硼酸的质量分数为(0.2728g÷0.3g) ×100%=90.93%;③若滴定时滴定管尖嘴部分有气泡,滴定过程中消失,则消耗的NaOH溶液的体积偏大,使硼酸的含量偏大。
考点:考查物质溶解使用的仪器、pH试纸的使用方法、离子方程式的书写、滴定终点的判断、物质含量的测定、误差分析的知识。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源:2015届江苏省中学高三上学期第一次月考化学试卷(解析版) 题型:选择题
常温下,对pH=10的NaHCO3溶液中,各微粒的物质的量浓度分析正确的是()
A.c(CO32—)>c(H2CO3)
B.c(Na+)>c(HCO3—)>c(OH―)>c(H+)
C.c(Na+)+c(H+)=c(HCO3—)+c(CO32—)+c(OH―)
D.c(Na+)=c(HCO3—)+c(CO32—)
查看答案和解析>>
科目:高中化学 来源:2015届江西南昌三中高三11月份月考化学试卷(解析版) 题型:选择题
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeCl2溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入过量CO2
A.①③④⑤ B.只有①④ C.只有②③ D.只有③④⑤
查看答案和解析>>
科目:高中化学 来源:2015届江苏连云港市高三上第一次月考化学试卷(解析版) 题型:选择题
某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是( )
A.①②③④ B.①②⑤⑥ C.③⑤⑥⑦ D.①③④⑦
查看答案和解析>>
科目:高中化学 来源:2015届江苏连云港市高三上第一次月考化学试卷(解析版) 题型:选择题
物质分类是化学研究的重要方法之一。化学工作者经常根据物质的组成对物质进行分类研究。近年来发现,在金星大气层中存在三氧化二碳。下列物质与它属于同类的是
A.H2、O3 B.H2SO4、H2CO3 C.SO2、NO D.Na2SO3、KClO3
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市高三上学期期中考试化学试卷(解析版) 题型:选择题
25℃时,0.1mol·L-1下列溶液的pH如下表,有关比较错误的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3C | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸的强度:HF>H2CO3
B.由水电离产生的c(H+):①=②
C.溶液中酸根离子浓度:c(F-)>c(HCO3-)
D.序号④中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.NaHCO3溶液中加入醋酸溶液:HCO3 -+ H+ = CO2↑+ H2O
-+ H+ = CO2↑+ H2O
B.NaAlO2溶液中通入过量CO2气体:2AlO2-+ CO2 +3H2O = 2Al(OH)3↓+CO32-
C.Fe(OH)2溶于足量稀硝酸:Fe(OH)2 + 2H+ = Fe2+ + 2H2O
D.乙醛与含有NaOH的Cu(OH)2悬浊液共热:CH3CHO + OH-+2Cu(OH)2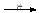 CH3COO-+ Cu2O↓+3H2O
CH3COO-+ Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
下列操作方法或实验装置正确的是

A.装置①探究NaHCO3的热稳定性 B.装置②HCl的收集
C.装置③乙醇的水溶液蒸馏 D.装置④检验K2CO3中的K+
查看答案和解析>>
科目:高中化学 来源:2015届河南省名校高三上学期期中考试理综化学试卷(解析版) 题型:填空题
有M、N两种溶液,经测定这两种溶液中大量存在下列12种离子:Al3+、Cl-、Na+、K+、NO3—、OH-、Fe2+、AlO2—、CO32—、NH4+、SO42—、H+。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
实验内容以及现象 | 结论 |
①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 |
|
②
| 确定M溶液中含有Na+,不含K+ |
③用pH试纸检测M溶液,pH试纸呈蓝色 |
|
(2)根据(1)中的实验回答:
NO3—存在于________溶液中,理由是 ;
Cl-存在于________溶液中,理由是 ;
(3)根据(1)中的实验确定,M溶液中含有的离子为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com