
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
分析 室温时,某溶液中由水电离生成的H+和OH-物质的量浓度的乘积为1×10-24,则水电离的氢离子、氢氧根离子浓度都是1×10-24,该溶液为酸性或碱性溶液,
A.四种离子之间不反应,都不与氢离子反应;
B.四种离子都不与氢氧根离子反应;
C.四种离子都不与氢离子反应;
D.铵根离子与氢氧根离子反应,硅酸根离子与氢离子反应,铵根离子与硅酸根离子发生双水解反应.
解答 解:室温时,某溶液中由水电离生成的H+和OH-物质的量浓度的乘积为1×10-24,则水电离的氢离子、氢氧根离子浓度都是1×10-24,该溶液为酸性或碱性溶液,
A.Al3+、Na+、NO3-、Cl-之间不反应,都不与氢离子反应,在酸性溶液中能够共存,故A错误;
B.K+、Na+、Cl-、CO32-之间不反应,都不与氢氧根离子反应,在碱性溶液中能够共存,故B错误;
C.NH4+、Na+、Cl-、SO42-之间不反应,都不与氢离子反应,在酸性溶液中能够大量共存,故C错误;
D.NH4+与氢氧根离子反应,SiO32-与氢离子反应,NH4+、SiO32-之间发生双水解反应,在溶液中一定不能大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

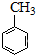 $→_{水溶加热}^{浓H_{2}SO_{4}浓HNO_{3}}$
$→_{水溶加热}^{浓H_{2}SO_{4}浓HNO_{3}}$
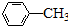 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$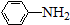 (弱碱性,易被氧化)
(弱碱性,易被氧化) .
.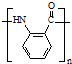 .
. 水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构.
水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构. →B
→B 等.
等. 的同分异构体:
的同分异构体: 、
、 等
等 属于不同类别
属于不同类别 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用催化剂可将汽车尾气中的NO、CO转化为无毒的气体 | |
| B. | 化石燃料的过量使用加剧了雾霾天气及空气中的PM2.5 | |
| C. | 小苏打是制作馒头和面包的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 蛋白质溶液中加入饱和Na2SO4溶液或CuSO4溶液,析出固体原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
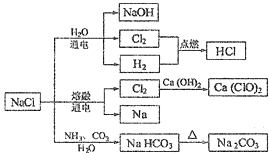
| A. | 常温时,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应可用于制备漂白粉,漂白粉的主要成分是Ca(ClO)2和CaCl2 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷燃烧 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在镍做催化剂的条件下,苯与氢气反应 | |
| D. | 乙烷与氯气在光照下反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气中含有的少量氯化氢,可用氢氧化钠溶液除去 | |
| B. | NaHCO3的热稳定性比Na2CO3强 | |
| C. | 过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+ | |
| D. | 氨气喷泉实验说明氨气极易溶解于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | 需加入的试剂 | 有关离子方程式 |
| FeSO4 (Fe2(SO4)3) | ||
| Mg(Al) | ||
| CO2 (HCl) | ||
| SiO2(CaCO3) | . |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com