
【题目】镁化合物具有广泛用途。请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的____,还生成少量的______(填化学式);
(2)CH3MgCl是一种重要的有机合成试剂,其中镁的化合价是___________,该化合物水解的化学方程式为____________;
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
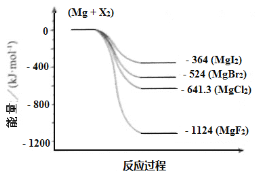
下列选项中正确的是_____________(填序号)。
① MgI2中Mg2+ 与I- 间的作用力小于MgF2中Mg2+ 与F- 间的作用力
② Mg与F2的反应是吸热反应
③ MgBr2与Cl2 反应的△H > 0
④ 化合物的热稳定性顺序为MgI2 < MgBr2 < MgCl2 < MgF2
⑤ MgF2(s) + Br2(l) = MgBr2(s) + F2(g) △H = +600 kJ · mol-1
【答案】 MgO Mg3N2 +2 2CH3MgCl + 2H2O = 2CH4↑+ MgCl2 + Mg(OH)2 ①④⑤
【解析】(1)镁在空气中燃烧,镁和氧气反应生成氧化镁,和氮气反应生成氮化镁,所以单质镁在空气中燃烧的主要产物是白色的氧化镁,还生成少量的氮化镁;(2)CH3MgCl中,Cl元素的化合价是-1价,H元素的化合价是+1价,C元素的化合价是-4价,所以镁元素的化合价是+2价,CH3MgCl水解生成氢氧化镁、氯化氢和甲烷,水解方程式为:CH3MgCl+2H2O=Mg(OH)2↓+CH4↑+HCl;(3)①相同类型的离子晶体中,离子键越大,则离子间作用力越强,物质含有的能量越低,所以MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力,正确;②根据图象知,反应物的能量大于生成物能量,所以Mg与F2的反应是放热反应,错误;③氯化镁的能量小于溴化镁的能量,氯气的能量大于溴的能量,所以MgBr2与Cl2反应是放热反应,即△H<0,错误;④能量越小的物质越稳定,所以化合物的热稳定性顺序为MgI2<MgBr2<MgCl2<MgF2,正确;⑤已知:Mg(s)+F2(l)=MgF2(s)△H=-1124kJ/mol,
Mg(s)+Br2(l)=MgBr2(s)△H=-524kJ/mol,将第二个方程式与第一方程式相减得MgF2(s)+Br2(l)=MgBr2(s)+F2(g)△H=+600kJmol-1,正确;答案选①④⑤。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置关系如右图所示,其中Z元素原子的最外层电子数是其电子层数的2倍。
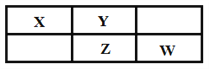
请回答下列问题:
(1)元素Z位于周期表中第_______周期,________族;
(2)这些元素的最高价氧化物对应的水化物中,水溶液酸性最强的是_______(写化学式);
(3)Y和Z组成的化合物的化学式为_______;
(4)W的单质和过量的X的氢化物可发生氧化还原反应,所得两种产物的电子式分别为____________、___________;
(5)W的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol 电子转移时,共产生9 mol 气体,写出该反应的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,体积不变的密闭容器中,对可逆反应A(g) + 2B(g)![]() 3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
A. 单位时间内消耗a mol A,同时生成3a mol C
B. C的生成速率与C的分解速率相等
C. 混合气体的总物质的量不再变化
D. 容器内的压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是
A.NH4+ 、Ag+、PO43-、Cl- B.Fe3+、H+、I-、HCO3-
C.K+、Na+、NO3- 、MnO4- D.Al3+、Mg2+ 、SO42- 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将硅粉与镁粉混合后隔绝空气强热,得到一种暗蓝色的化合物。将此化合物投入水中,发生剧烈反应,产生气体,并伴有爆炸声与火光。此过程不可能发生的反应是:
A. 2Mg + Si![]() Mg2Si B. Mg2Si + 4H2O = 2Mg(OH)2 + SiH4↑
Mg2Si B. Mg2Si + 4H2O = 2Mg(OH)2 + SiH4↑
C. SiO2 + H2O = H2SiO3 D. SiH4 + 2O2 = SiO2 + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B_________________;沉淀D __________________;
溶液E_________________________________________。
(3)写出①、④两个反应的化学方程式
①__________________________________;④_____________________________。
(4)写出②、③两个反应的离子方程式
②_________________________________;③______________________________。
(5)设计实验检验溶液F中所含溶质:______________________________________
(6)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3__________________________Fe2O3____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解H2SO4和NaCl的混合溶液,起始一段时间阴极和阳极上分別析出的物质是
A. H2、O2 B. Cu、O2 C. H2、Cl2 D. Cu、Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是

A. 该装置将化学能转化为电能
B. 为了增加灯泡亮度,可以将电极碳棒变得粗糙多孔
C. 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a
D. 该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com