
取一定质量的纯MnO2和纯KClO3混合并加热,使其充分反应.将剩余固体与足量浓盐酸再混合加热,反应完毕后将溶液蒸干,此时得到的固体质量与原MnO2、KClO3混合物质量相等.求KClO3在原混合物中的质量分数.
|
解:2KClO3 设原混合物中KClO3的物质的量为n(KClO3),MnO2的物质的量n(MnO2),则生成KCl的物质的量与KClO3相等n(KCl)=n(KClO3),MnCl2的物质的量与MnO2的物质的量相等,n(MnCl2)=n(MnO2) 根据题意得:n(KCl)·M(KCl)+n(MnCl2)·M(MnCl2)=n(KClO3)·M(KClO3)+n(MnO2)·M(MnO2) 即n(KClO3)×(122.5-74.5)=n(MnO2)×(126-87) n(KClO3)∶n(MnO2)=39∶48 原混合物中KClO3的质量分数w(KClO3)= 答:略. |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 温度 溶解度 化学式 |
0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| KClO4 | 0.76 | 1.06 | 1.68 | 2.56 | 3.73 |
| KCl | 28 | 31.1 | 34.2 | 37.2 | 40.1 |
| NaClO4 | 167 | 183 | 201 | 222 | 245 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
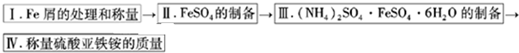
| 温度/℃ | FeSO4?7H2O | (NH4)2SO4 | (NH4)2SO4?FeSO4?6H2O |
| 10 | 20.0 | 73.0 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78.0 | 28.1 |
查看答案和解析>>
科目:高中化学 来源:走向清华北大同步导读·高一化学 题型:038
取一定质量两种钠的正盐A、B,放入1 L 0.2mol/L HCl溶液中(设加钠盐前后溶液体积不变)得固体C和溶液D.经过滤(设D全部进入滤液)、洗涤(弃去洗涤液)、干燥后,取C的![]() 使之在空气中燃烧,并把燃烧产物E全部通入D溶液,又得固体C(质量和前次所得相同)及溶液F,把A、B或E加入F溶液均未见固体生成.测得溶液中的H+浓度为0.1mol/L.问:
使之在空气中燃烧,并把燃烧产物E全部通入D溶液,又得固体C(质量和前次所得相同)及溶液F,把A、B或E加入F溶液均未见固体生成.测得溶液中的H+浓度为0.1mol/L.问:
(1)写出A、B、C、E物质的化学式,A、B各多少摩尔?
(2)D、F溶液中溶质各为何物?它们的物质的量各是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定K2CO3和NaHCO3混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的Ba(OH)2溶液,每次实验均充分反应,实验结果记录如下表:
| 实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
| 1 | 0.858 | 0.5 | 1.379 |
| 2 | 1.716 | 0.5 | |
| 3 | 2.574 | 0.5 | 4.137 |
| 4 | 3.432 | 0.5 | 5.516 |
| 5 | 4.290 | 0.5 | 5.516 |
| 6 | 5.148 | 0.5 | 5.516 |
请回答下列问题:
(1)第二次实验中产生沉淀的质量是 g。
(2)混合物中K2CO3和NaHCO3的物质的量之比为 。
(3)在25℃时,取下第3组实验所得溶液体积的1/10,加水配成500mL溶液,求此溶液pH。(本小题要求写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com