
【题目】在氯化氢分子中,形成共价键的原子轨道是( )
A.氯原子的2p轨道和氢原子的1s轨道
B.氯原子的2p轨道和氢原子的2p轨道
C.氯原子的3p轨道和氢原子的1s轨道
D.氯原子的3p轨道和氢原子的3p轨道
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,向体积恒定为2L的密闭容器里充人2molM和一定量的N发生如下反应M(g)+N(g)E(g)。当反应进行到4min时达到平衡,测知M的浓度为0.2mol L-1。下列说法不正确的是( )
A. 2min时,M的物质的量浓度为0.6molL-1
B. 4min时,用M表示的反应速率为0.2 molL-1
C. 4min后,向容器中充入不参与反应的稀有气体,M的物质的量不变
D. 4min时,M的转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图装置可以完成一系列实验(图中夹持装置及加热装置已略去),不考虑①②③中物质间的相互影响。请回答下列问题:
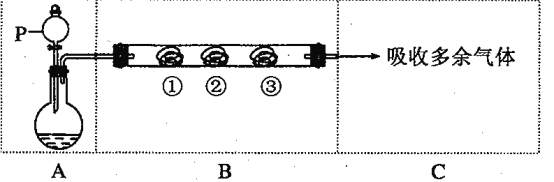
(1)若装置A选用浓盐酸和二氧化锰混合制取Cl2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
B中棉花的位置 | ① | ② | ③ |
所蘸试剂 | 石蕊溶液 | 淀粉KI溶液 | 浓氨水 |
现象 | ________ | ________ | ________ |
涉及的化学方程式 | ________ | ________ | 3Cl2+8NH3=6NH4Cl+N2 |
(2)若装置A选用浓硫酸和亚硫酸钠固体制取SO2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
B中棉花的位置 | ① | ② | ③ |
所蘸试剂 | H2S溶液 | 酸性KMnO4溶液 | 品红溶液 |
现象 | ________ | ________ | 褪色 |
体现SO2的性质 | ________ | ________ | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH=1的强酸溶液,加水稀释后,溶液中所有离子的浓度均降低。
②pH=2的盐酸和pH=1的醋酸,c(H+)之比为2∶1。
③在Na2CO3和NaHCO3溶液中均存在下列关系c(Na+)+c(H+)=c(OH-)+c(HCO3)+2c(CO32-)
④反应2A (s) + B (g)=2C (g) + D (g) 不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw;
则三者关系为:Ka·Kh=Kw
⑥反应A(g)![]() 2B(g);△H,若正反应的活化能为Ea kJ·mol-1,逆反应的活化能为Eb kJ·mol-1,则△H =(Ea -Eb)kJ·mol-1。其归纳正确的是
2B(g);△H,若正反应的活化能为Ea kJ·mol-1,逆反应的活化能为Eb kJ·mol-1,则△H =(Ea -Eb)kJ·mol-1。其归纳正确的是
A.①②③⑥ B.③④⑤⑥ C.②④⑤⑥ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列装置可以完成的实验组合是
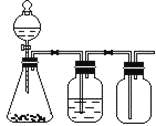
选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
C | Zn 稀硫酸 | 浓硫酸 | H2 |
D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
A. AB. BC. CD. D
【答案】B
【解析】
A. 二氧化锰与氯酸钾制取氧气,属于固体加热型,锥形瓶没有加热,所以不能用图中实验装置制取,选项A错误;
B.大理石与盐酸生成二氧化碳气体,属于固液常温型,盐酸有挥发性,挥发的HCl能与碳酸氢钠溶液反应产生二氧化碳气体,且二氧化碳密度比空气的大,能用向上排空气法收集;选项B正确。
C.锌粒与稀硫酸反应生成氢气,属于固液常温型,但氢气密度比空气的小,不能用向下排空气法收集,选项C错误;
D. 二氧化锰与浓盐酸制取氯气,属于固体加热型,锥形瓶没有加热,所以不能用图中实验装置制取,选项D错误;
故合理选项是B。
【题型】单选题
【结束】
20
【题目】下列物质中,不可作漂白剂的是( )
A. SO2 B. Ca(ClO)2 C. Na2SiO3 D. NaClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25 ℃时:
①HF(aq)+OH-(aq)===F-(aq)+H2O(l) ![]() H=-67.7 kJ·mol-1
H=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)===H2O(l) ![]() H=-57.3 kJ·mol-1
H=-57.3 kJ·mol-1
在20 mL 0.1 mol·L-1氢氟酸中加入V mL 0.1 mol·L-1 NaOH溶液,下列有关说法正确的是( )
A.氢氟酸的电离方程式及热效应可表示为:HF(aq)![]() F-(aq)+H+(aq)
F-(aq)+H+(aq) ![]() H=+10.4 kJ·mol-1
H=+10.4 kJ·mol-1
B.当V=20时,溶液中:c(OH-)=c(HF)+c(H+)
C.当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol·L-1
D.当V>0时,溶液中一定存在:c(Na+)>c(F-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质或指定物质主要成分与化学式对应正确的是
A. 明矾 Al2(SO4)312H2OB. 漂白粉 CaClO
C. 纯碱 NaHCO3D. 水煤气 CO、H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从石油中裂解获得A是目前工业上生产A的主要途径,图中的N是高分子化合物。以A和1,3一丁二烯为原料合成N的流程如下:
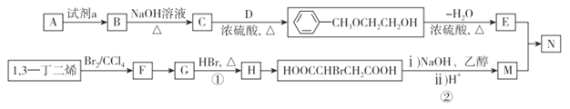
请回答下列问题:
(1)D物质的名称为_____;B→C的化学反应方程式为_____________。
(2)G中官能团的名称为_____________,由C→E涉及到的反应类型为_________。
(3)在催化剂存在下,E和M等物质的量发生聚合反应,N的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 在NH4+和[Cu(NH3)4]2+中都存在配位键
B.  σ键和π键比例为7:1
σ键和π键比例为7:1
C. ![]() 与
与![]() 互为等电子体,1 mol
互为等电子体,1 mol ![]() 中含有的π键数目为2NA
中含有的π键数目为2NA
D. 已知反应N2O4(l)+2N2H4(l) = 3N2(g)+4H2O(l),若该反应中有4 mol N—H键断裂,则形成的π键数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com