
【题目】设NA为阿伏伽德罗常数的值。下列说法错误的是
A. 相同质量的CO与N2,所含分子数、原子数均相同
B. 56 g乙烯中所含共用电子对数目为12NA
C. 31 g白磷中所含共价键数目为NA
D. 14 g乙烯与丙烯的混合气体中所含氢原子数目为2NA
【答案】C
【解析】
A项,CO和N2的摩尔质量均为28g/mol,均为双原子分子;B项,从乙烯的电子式(![]() )可看出,1mol乙烯含有6mol共用电子对;C项,白磷分子是由四个磷原子构成的正四面体 分子式是P4,白磷分子中含有6个P-P共价键,据此进行计算含有共价键数目;D项,乙烯与丙烯的最简式都是CH2,以此进行分析解决。
)可看出,1mol乙烯含有6mol共用电子对;C项,白磷分子是由四个磷原子构成的正四面体 分子式是P4,白磷分子中含有6个P-P共价键,据此进行计算含有共价键数目;D项,乙烯与丙烯的最简式都是CH2,以此进行分析解决。
A项,CO和N2的摩尔质量均为28g/mol,均为双原子分子,所以相同质量的CO与N2,物质的量相同,所含分子数、原子数均相同,故A正确;B项,1mol乙烯含有共用电子对为6NA,56 g乙烯的物质的量为2mol,则含有共用电子对数目为12NA,故B正确;C项,白磷是正四面体结构,分子中含有6个P-P共价键,31g白磷(P4)的物质的量是0.25mol,所以分子中含有P-P共价键1.5mol,即含有的共价键数目为1.5 NA,故C错误;D项,乙烯与丙烯的最简式都是CH2,14 g乙烯和丙烯混合气体中的氢原子数为:![]() =2NA,故D正确。综上所述,符合题意的选项为C。
=2NA,故D正确。综上所述,符合题意的选项为C。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】随着工农业发展,NH4Cl的需求显著降低,价格低迷和产品积压导致利用“侯氏制碱法”生产的碱厂出现亏损。新联合制碱法在此基础上将氯元素转化为更有应用价值的HCl。

(1)气体X是__________。
(2)已知25℃时部分物质的溶解度数据:
物质 | NaCl | NaHCO3 | NH4Cl | NH4HCO3 |
溶解度/g | 36.0 | 10.3 | 39.5 | 24.8 |
结合表中数据说明过程Ⅰ中的反应能发生的原因是______________。
(3)过程Ⅰ获得的NaHCO3会吸附微量NH4Cl,导致产品Na2CO3中混有NaCl。
①用化学方程式表示过程Ⅱ中NaCl生成的原因:_____________。
②检验Na2CO3中NaCl的实验操作是,取少量固体于试管中_____________。
(4)过程Ⅲ以MgO为催化剂,在不同温度下加热灼烧,将NH4Cl分解为NH3和HCl。

①步骤i中反应的化学方程式是____________。
②过程Ⅲ的优点是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤产生的SO2会污染空气。某实验小组用下图装置(夹持仪器略、气密性好)探究SO2的性质,并研究治理措施。

(1)装置①中反应的化学方程式是_______________。
(2)从物质类别的角度分析,SO2和CO2具有相似的化学性质,欲验证该性质,②中可选用的试剂及预期的实验现象是_________________。
(3)当②中为氢硫酸(溶质为H2S)时,观察到②中出现黄色沉淀,说明SO2具有的化学性质是_______________。
(4)当②中为碘水时,观察到②中溶液由黄色变为无色,由此推测所得无色溶液中的离子主要是H+、I-和_________;通过进一步实验证实了该过程中SO2已被氧化,实验操作及现象是______________。
(5)结合SO2的性质,请你针对煤的使用及其产生的环境污染提出一条解决或缓解的建议:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置图中的实验方案能达到实验目的的是
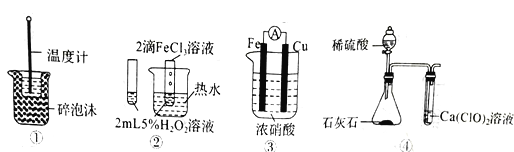
A. 图①可用于中和热的测定
B. 图②可验证FeCl3对H2O2分解反应有催化作用
C. 图③可用于探究铁作负极的原电池原理
D. 图④可用于验证酸性:H2SO4>H2CO3>HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备,正丁烷(C4H10)催化脱氢制1-丁烯(C4H8) 的化学方程式如下:C4H10(g)=C4H8(g)+H2(g)△H,如图是该反应平衡转化率与反应温度及压强的关系图,下列说法正确的是
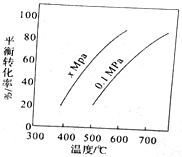
A. x>0.1
B. △H>O
C. 500C时,压强xMPa比0.1MPa条件下的平衡常数大
D. 一定温度下,在一恒容密闭容器中发生该反应,C4H10的浓度越高,平衡转化率越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,其原子序数依次增大。其中A元素原子核内只有一个质子;A与C、B与D分别同主族;B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。
请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是____(填字母)。
A.A2B B.DB2 C.E2 D.C2DB3
(2)D元素在元素周期表中的位置为____;化合物C2B中两种离子的半径大小关系为(填离子符号,下同)_________>____。
(3)实验室中欲选用如图所示装置制取并收集纯净干燥的E2气体。
①实验中应选用的装置为_______(按由左到右的连接顺序填写)。
②装置A中发生反应的离子方程式为______。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。

(1)B装置中的干燥剂是_____(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是_____(填”C”或“D”)。
(3)当实验进行段时间后,挤压E装置中的胶头滴管,滴入1--2滴浓盐酸,可观察到E装置中的现象是产生______(填”烟”或“白雾”)。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____(填“F”或“G”)。
(5)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是____(填“a”“b”或“c”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com