
”¾ĢāÄæ”æ³£ĪĀĻĀ,ÓƵČÅØ¶ČµÄNaOHČÜŅŗ·ÖeµĪ¶ØĻąĶ¬Ģå»żµÄNH4Cl”¢KH2PO4¼°CH3COOHČÜŅŗ£¬µĪ¶ØĒśĻßČēĻĀĶ¼ĖłŹ¾:
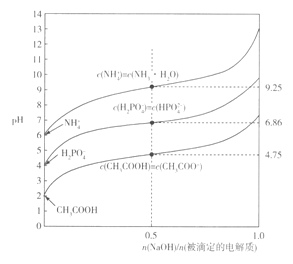
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. NH3”¤H2O===NH4++OH-µÄlg K =-9.25
B. 0.1mol/LKH2PO4ČÜŅŗÖŠ:c( HPO42- )<c(H3PO4)
C. CH3COOH+HPO42-=CH3COO-+H2PO4-µÄlg K = -11.61
D. ŌŚµĪ¶Ø¹ż³ĢÖŠ£¬µ±ČÜŅŗpHĻąĶ¬Ź±,ĻūŗÄNaOH µÄĪļÖŹµÄĮæ:CH3COOH>KH2PO4> NH4Cl
”¾“š°ø”æD
”¾½āĪö”æA.ÓÉĶ¼ĻóæÉÖŖ£¬µ±¼ÓČėµÄĒāŃõ»ÆÄĘÓė±»µĪ¶ØNH4ClĪļÖŹµÄĮæÖ®±ČĪŖ1:2Ź±£¬n(NH4+)=n(NH3![]() H2O),NH3”¤H2O
H2O),NH3”¤H2O![]() NH4++OH-µÄĘ½ŗā³£ŹżK=c(NH4+)c(OH-)/c(NH3.H2O)=c(OH-)=10-14/10-9.25=10-4.75,lgK=-4.75,¹ŹA“ķ£»B.ÓÉÓŚKH2PO4ČÜŅŗµÄpHĪŖ4£¬ĖµĆ÷H2PO4-µēĄė“óÓŚĖ®½ā£¬ĖłŅŌc(HPO42-)>c(H3PO4),¹ŹB“ķ£»C.CH3COOH+HPO42-
NH4++OH-µÄĘ½ŗā³£ŹżK=c(NH4+)c(OH-)/c(NH3.H2O)=c(OH-)=10-14/10-9.25=10-4.75,lgK=-4.75,¹ŹA“ķ£»B.ÓÉÓŚKH2PO4ČÜŅŗµÄpHĪŖ4£¬ĖµĆ÷H2PO4-µēĄė“óÓŚĖ®½ā£¬ĖłŅŌc(HPO42-)>c(H3PO4),¹ŹB“ķ£»C.CH3COOH+HPO42-![]() CH3COO-+H2PO4-,Ę½ŗā³£ŹżK=
CH3COO-+H2PO4-,Ę½ŗā³£ŹżK=![]() =
=![]() £¬ÓĆŗĶĒóK(NH3
£¬ÓĆŗĶĒóK(NH3![]() H2O)Ķ¬ŃłµÄ·½·ØæɼĘĖć³öK(CH3COOH)=10-4.75£¬K(H2PO4-)=10-6.86£¬Ōņ
H2O)Ķ¬ŃłµÄ·½·ØæɼĘĖć³öK(CH3COOH)=10-4.75£¬K(H2PO4-)=10-6.86£¬Ōņ![]() =10-4.75/10-6.86=102.11,lgK=2.11,¹ŹC“ķĪó£»DĻī£¬“ÓĶ¼ĻńæÉÖŖ£¬ŌŚµĪ¶Ø¹ż³ĢÖŠ£¬µ±ČÜŅŗpHĻąĶ¬Ź±,ĻūŗÄNaOHµÄĪļÖŹµÄĮæ:CH3COOH>KH2PO4>NH4Cl£¬¹ŹDÕżČ·£»×ŪŗĻŅŌÉĻ·ÖĪö£¬±¾ĢāÕżČ·“š°øĪŖD”£
=10-4.75/10-6.86=102.11,lgK=2.11,¹ŹC“ķĪó£»DĻī£¬“ÓĶ¼ĻńæÉÖŖ£¬ŌŚµĪ¶Ø¹ż³ĢÖŠ£¬µ±ČÜŅŗpHĻąĶ¬Ź±,ĻūŗÄNaOHµÄĪļÖŹµÄĮæ:CH3COOH>KH2PO4>NH4Cl£¬¹ŹDÕżČ·£»×ŪŗĻŅŌÉĻ·ÖĪö£¬±¾ĢāÕżČ·“š°øĪŖD”£


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¬Ņ»¶ĢÖÜĘŚŌŖĖŲ¼×”¢ŅŅ”¢±ū”¢¶”Ō×ÓŠņŹżŅĄ“ĪŌö“󔣳£ĪĀĻĀ£¬ŗ¬¼×µÄ»ÆŗĻĪļrÅضČĪŖ0.1mol”¤L-1Ź±ČÜŅŗpH=13”£Ķ¬ÖÜĘŚŌŖĖŲ¼ņµ„Ąė×ÓÖŠ£¬ŅŅĄė×ӵİė¾¶×īŠ””£pŗĶq·Ö±šŹĒŌŖĖŲ±ūŗĶ¶”µÄµ„ÖŹ£¬ĘäÖŠpĪŖĒ³»ĘÉ«¹ĢĢ唣ÉĻŹöĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾(²śĪļĖ®ŅŃĀŌČ„)”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
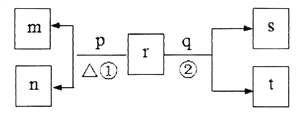
A. Ō×Ó°ė¾¶µÄ“󊔹ŲĻµ£ŗ¼×>ŅŅ>±ū>¶”
B. ·“Ó¦¢ŚµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗC12+H2O![]() H++C1-+HC1O
H++C1-+HC1O
C. m”¢nµÄŅõĄė×ÓŌŚĖįŠŌĢõ¼žĻĀ²»ÄÜ“óĮæ¹²“ę
D. ¼×”¢ŅŅ”¢¶”µÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĮ½Į½Ö®¼ä¾łæÉŅŌ·¢Éś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ÓĆ0.10 mol”¤L-1HClČÜŅŗµĪ¶Ø20 mL 0.050 mol”¤L-1Na2CO3ŗĶ0.025 mol”¤L-1NaHCO3»ģŗĻČÜŅŗ£¬µĆ³öČēĶ¼ĖłŹ¾µÄµĪ¶ØĒśĻß”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
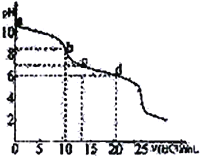
A. aµćČÜŅŗĻŌ¼īŠŌµÄÖ÷ŅŖŌŅņ£ŗCO32-+H2O![]() HCO3-+CH-
HCO3-+CH-
B. bµćČÜŅŗÖŠ£ŗc(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. cµćČÜŅŗÖŠ£ŗc(Na+)=c(HCO3-)+2c(CO32-)+ c(Cl-)
D. dµćČÜŅŗÖŠ£ŗc(Na+)> c(Cl-)> c(HCO3-)>c(H+)>c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚÄ³ĪļÖŹŹĒ·ńĪŖµē½āÖŹµÄÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
A.¹ĢĢåĀČ»ÆÄĘ²»µ¼µē£¬ĖłŅŌĀČ»ÆÄĘ²»ŹĒµē½āÖŹ
B.ĀČ»ÆĒāĖ®ČÜŅŗÄܵ¼µē£¬ĖłŅŌĀČ»ÆĒāŹĒµē½āÖŹ
C.SO2ČÜÓŚĖ®Äܵ¼µē£¬ĖłŅŌSO2ŹĒµē½āÖŹ
D.°±Ė®Äܵ¼µē£¬ĖłŅŌ°±Ė®ŹĒµē½āÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬²»ŹōÓŚµē½āÖŹµÄŹĒ
A.H2SO4B.KOHC.FeD.NaNO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚæÉÄę·“Ó¦2A(g)£«3B(g) ![]() 4C(g)£«2D(g)£¬ŌŚ²»Ķ¬Ģõ¼žĻĀµÄ»Æѧ·“Ó¦ĖŁĀŹČēĻĀ£¬ĘäÖŠ±ķŹ¾µÄ·“Ó¦ĖŁĀŹ×īæģµÄŹĒ
4C(g)£«2D(g)£¬ŌŚ²»Ķ¬Ģõ¼žĻĀµÄ»Æѧ·“Ó¦ĖŁĀŹČēĻĀ£¬ĘäÖŠ±ķŹ¾µÄ·“Ó¦ĖŁĀŹ×īæģµÄŹĒ
A. v(A)£½0.9 mol”¤L£1”¤min£1 B. v(B)£½1.5 mol”¤L£1”¤min£1
C. v(D)£½0.8 mol”¤L£1”¤min£1 D. v(C)£½0.1 mol”¤L£1”¤s£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放»Æѧ-Ń”ŠŽ3:ĪļÖŹ½į¹¹ÓėŠŌÖŹ”æĆĢ¼°Ęä»ÆŗĻĪļÓĆĶ¾·Ē³£¹ć·ŗ”£»Ų“šĻĀĮŠĪŹĢā:
(1)Al70Pd21Mn9ŹĒŅ»ÖÖ×¼¾§Ģå(½éÓŚ¾§ĢåŗĶ·Ē¾§ĢåÖ®¼äµÄ¹ĢĢå),ÄÜ×¼Č·Ö¤Ć÷Ęä²»ŹĒ¾§ĢåµÄ·½·ØŹĒ___________”£
(2)»łĢ¬MnŌ×ӵļŪµē×ÓÅŲ¼Ź½ĪŖ_________,Ī“³É¶Ōµē×ÓŹżĪŖ_____øö”£
(3)MnSČŪµć(1610”ę)±ČMnOČŪµć(1650”ę)µĶ,ĘäŌŅņŹĒ____________”£
(4)ĆĢµÄŅ»ÖÖÅäŗĻĪļµÄ»ÆѧŹ½ĪŖ[Mn(CO)5(CH3CN)]Br”£
¢ŁÅäŗĻĪļÖŠĆĢŌŖĖŲµÄ¼ŪĢ¬ĪŖ________”£
¢ŚÅäĢåCH3CNÓėÖŠŠÄŌ×ÓŠĪ³ÉÅäĪ»¼üŹ±,Ģį¹©¹Ā¶Ōµē×ÓµÄŌ×ÓŹĒ_____,øĆ·Ö×ÓÖŠĢ¼Ō×ÓµÄŌӻƷ½Ź½ĪŖ_______£»C”¢H”¢NµÄµēøŗŠŌ“ӓ󵽊”µÄĖ³ŠņĪŖ________”£
(5)ĆĢµÄŗ¬ŃõĖįÓŠHMnO4(øßĆĢĖį)”¢H2MnO3(ŃĒĆĢĖį),øßĆĢĖįµÄĖįŠŌ±ČŃĒĆĢĖįĒæ,ĄķÓÉŹĒ_________”£
(6)ijÖÖŗ¬ĆĢĢŲŹā²ÄĮĻµÄ¾§°ū½į¹¹ČēĻĀĶ¼ĖłŹ¾:
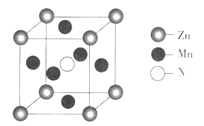
Čō¾§°ū²ĪŹżĪŖanm,ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ,ŌņøĆ¾§°ūµÄĆܶČĪŖ____(ĮŠ³ö“śŹżŹ½¼“æÉ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÖŠæÉÄÜŗ¬ÓŠH+”¢Mg2+”¢NH4+”¢Al3+”¢Fe3+”¢CO32”Ŗ”¢SO42”ŖÖŠµÄ¼øÖÖ”£Čō¼ÓČėŠæĮ£,²śÉśĪŽÉ«ĪŽĪ¶µÄĘųĢå;Čō¼ÓČėNaOHČÜŅŗ,²śÉś°×É«³Įµķ,ĒŅ²śÉśµÄ³ĮµķĮæÓė¼ÓČėNaOHµÄĪļÖŹµÄĮæÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ŌņĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
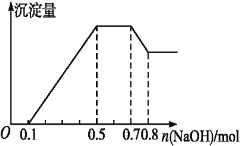
A. ČÜŅŗÖŠµÄŃōĄė×ÓÓŠH+”¢Mg2+”¢NH4+”¢Al3+
B. ČÜŅŗÖŠn(Al3+)=0.1 mol
C. ČÜŅŗÖŠŅ»¶Ø²»ŗ¬CO32”Ŗ,æÉÄÜŗ¬ÓŠSO42”Ŗ
D. n(H+)”Ćn(Al3+)”Ćn(Mg2+)=2”Ć2”Ć1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬Ļņa LĆܱÕČŻĘ÷ÖŠ¼ÓČė1mol XĘųĢåŗĶ2mol YĘųĢ壬·¢ÉśČēĻĀ·“Ó¦£ŗX(g)+2Y(g) ![]() 2Z(g)£¬“Ė·“Ó¦“ļµ½Ę½ŗāµÄ±źÖ¾ŹĒ
2Z(g)£¬“Ė·“Ó¦“ļµ½Ę½ŗāµÄ±źÖ¾ŹĒ
A£®ČŻĘ÷ÄŚĘųĢåĆÜ¶Č²»Ėꏱ¼ä±ä»Æ
B£®v (X): v (Y)= l£ŗ2
C£®ČŻĘ÷ÄŚX”¢Y”¢ZµÄÅØ¶Č²»Ėꏱ¼ä±ä»Æ
D£®µ„Ī»Ź±¼äĻūŗÄ0.1 molXĶ¬Ź±Éś³É0.2molZ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com