
25℃时,水的电离可达到平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
|
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH﹣)降低 |
|
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
|
| C. | 向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低 |
|
| D. | 将水加热,Kw增大,pH不变 |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
水的电离达到平衡:H2O⇌H++OH﹣,加入与H+或OH﹣反应的物质,改变c(OH﹣)或c(H+),可使平衡发生移动,KW只与温度有关.
解答:
解:A.向水中加入稀氨水溶液,平衡逆向移动,但c(OH﹣)升高,故A错误;
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW只与温度有关,温度不变,则KW不变,故B正确;
C.向水中加入少量醋酸,氢离子浓度增大,平衡逆向移动,故C错误;
D.水的电离为吸热反应,加热促进电离,则KW增大,pH变小,故D错误;
故选B.
点评:
本题考查弱电解质的电离,侧重于水的电离的考查,注意把握影响水的电离的因素以及水的离子积常数的特点.


科目:高中化学 来源: 题型:
某酸HX的稀溶液和某碱YOH的稀溶液的物质的量浓度相等,两溶液混合后,溶液的PH大于7,表中判断合理的是( )
| 编号 | HX | YOH | 溶液的体积关系 |
| ① | 强酸 | 强碱 | V(HX)=V(YOH) |
| ② | 强酸 | 强碱 | V(HX)<V(YOH) |
| ③ | 强酸 | 弱碱 | V(HX)=V(YOH) |
| ④ | 弱酸 | 强碱 | V(HX)=V(YOH) |
|
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
具有下列电子层结构的原子,其第一电离能由大到小排列正确的是
①3p轨道上只有一对成对电子的原子;②外围电子构型为3s23p6的原子;
③其3p轨道为半满的原子;④正三价的阳离子结构与氖相同的原子。
| A.①②③④ | B.③①②④ | C.②③①④ | D.②④①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列几种氢键:①O—H…O、②N—H…N、③F—H…F、④O—H…N,按氢键从强到弱的顺序正确的是
| A.③>①>④>② | B.①>②>③>④ |
| C.③>②>①>④ | D.①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
当Mg(OH)2在水中达到溶解平衡时:Mg(OH)2(s)⇌Mg2+(aq)+2OH﹣(aq)要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是( )
|
| A. | NH4Cl | B. | NaOH | C. | Na2CO3 | D. | Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,下列混合溶液的pH一定小于7的是( )
|
| A. | pH=3的盐酸和pH=11的氨水等体积混合 |
|
| B. | pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
|
| C. | pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
|
| D. | pH=3的硫酸和pH=11的氨水等体积混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
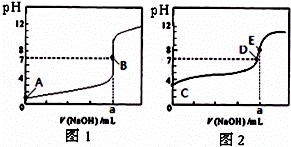
常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL 0.1000mol/L 盐酸和20.00mL 0.1000mol/L 醋酸溶液,得到2条滴定曲线,如图所示.若以HA表示酸,下列说法正确的是( )
|
| A. | 滴定盐酸的曲线是图2 |
|
| B. | 达到B、D状态时,两溶液中离子浓度均为 c(Na+)=c(A﹣) |
|
| C. | 达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl) |
|
| D. | 当0 mL<V(NaOH)<20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为 c(A﹣)>c(Na+)>c(H+)>c(OH﹣) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com