
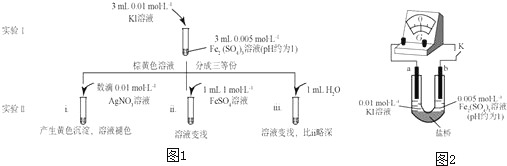
分析 (1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到化学平衡状态;
(2)根据实验iii和实验ii的对比可以看出是为了排除有ii中水造成溶液中离子浓度改变的影响;
(3)i.加入AgNO3,Ag+与I-生成AgI黄色沉淀,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动;
ii.加入FeSO4,Fe2+浓度增大,平衡逆移;
①K闭合时,指针向右偏转,可知b极Fe3+得到电子,作正极;
②当指针归零(反应达到平衡)后,向U型管左管中滴加0.01mol/L AgNO3溶液,若生成黄色沉淀,可知I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动;
(5)①Fe2+浓度增大,还原性增强;
②与(4)实验对比,不同的操作是当指针归零(反应达到平衡)后,向U型管右管中滴加0.01mol/L FeSO4溶液;
(6)将(3)和(4)、(5)作对比,可知氧化性、还原性与浓度有关.
解答 解:(1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到化学平衡状态,否则干扰平衡移动的判断,故答案为:化学平衡状态;
(2)由实验iii和实验ii的对比可知,对比实验的目的是为了排除有ii中水造成溶液中离子浓度改变的影响,故答案为:溶液稀释对颜色的变化;
(3)i.加入AgNO3,Ag+与I-生成AgI黄色沉淀,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动,可知Fe2+向Fe3+转化,故答案为:Ag+与I-生成AgI黄色沉淀,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动;
ii.加入FeSO4,Fe2+浓度增大,平衡逆移;
①K闭合时,指针向右偏转,右侧为正极,可知b极Fe3+得到电子,则b作正极,故答案为:正;
②当指针归零(反应达到平衡)后,向U型管左管中滴加0.01mol/L AgNO3溶液,若生成黄色沉淀,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动,指针向左偏转,也可证明推测Fe2+向Fe3+转化,故答案为:左管出现黄色沉淀,指针向左偏转;
(5)①转化的原因为Fe2+浓度增大,还原性增强,使Fe2+还原性强于I-,
故答案为:Fe2+浓度增大,还原性增强,使Fe2+还原性强于I-;
②与(4)实验对比,不同的操作是当指针归零(反应达到平衡)后,向U型管右管中滴加0.01mol/L FeSO4溶液,Fe2+向Fe3+转化,
故答案为:向U型管右管中滴加0.01mol/L FeSO4溶液;
(6)将(3)和(4)、(5)作对比,得出的结论是该反应为可逆的氧化还原反应,在平衡时,通过改变物质的浓度,可以改变物质的氧化、还原能力,并影响平衡移动,
故答案为:该反应为可逆的氧化还原反应,在平衡时,通过改变物质的浓度,可以改变物质的氧化、还原能力,并影响平衡移动.
点评 本题为2015年北京高考真题,侧重原电池、氧化还原反应及平衡移动的综合考查,把握平衡移动的影响因素及物质的性质为解答的关键,对分析与实验能力要求较高,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. |  | B. | HOOC-COOH | C. | HOCH2CH2OH | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H20 | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-═ClO-+Cl?+H2O | |
| B. | 该消毒液的pH约为12:ClO-+H2O?HClO+OH-? | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-═Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-═HClO+CH3COO-? |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
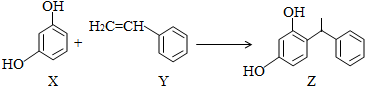
| A. | X、Y和Z均能使溴水褪色 | |
| B. | X和Z均能与NaHCO3溶液反应放出CO2 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
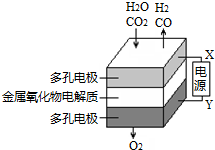 在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2e-═H2+O2-,CO2+2e-═CO+O2- | |
| C. | 总反应可表示为:H2O+CO2$\frac{\underline{\;通电\;}}{\;}$H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO、MgO、Na2O2均属于碱性氧化物 | B. | 盐酸、醋酸、苯酚均属于强电解质 | ||
| C. | CO2、CCl4、蛋白质均属于有机物 | D. | 液氯、晶体硅、臭氧均属于单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com