
| A. | 体系的压强不再发生变化 | |
| B. | 气体密度不再发生变化 | |
| C. | 生成nmol CO的同时消耗n mol H2O | |
| D. | 1 molH一H键断裂的同时断裂2 mol H-O键 |
分析 可逆反应C(s)+H2O(g)═CO(g)+H2(g)达到平衡状态时,正逆反应速率相等,各组分的浓度、百分含量不再变化,注意C的状态为固态.
解答 解:A.该反应为气体体积增大的反应,压强为变量,当体系的压强不再发生变化,说明正逆反应速率相等,反应达到平衡状态,故A不选;
B.反应中C为固态,反应前后气体质量发生变化,容器容积不变,则密度为变量,当气体密度不再发生变化时,表明各组分的浓度不再变化,反应达到平衡状态,故B不选;
C.生成nmol CO的同时消耗n mol H2O,表示的都是正反应速率,无法判断该反应是否达到平衡状态,故C选;
D.1 molH-H键断裂的同时断裂2 mol H-O键,表示的是正逆反应速率,且满足计量数关系,说明该反应已经达到平衡状态,故D不选;
故选C.
点评 本题考查化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,B为易错点,注意C的状态为固体,试题培养了学生的灵活应用能力.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:解答题
 消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题.
消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题.| t/min n(NO)/mol T | 0 | 40 | 80 | 120 | 160 | |
| 甲 | T℃ | 2 | 1.45 | 1 | 1 | 1 |
| 乙 | 400℃ | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
| 丙 | 400℃ | 1 | 0.8 | 0.65 | 0.53 | 0.45 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | c(Na+)>2c(CO32-) | B. | C(Na+)+c(H+)═c(HCO3-)+c(OH-)+c(CO32-) | ||
| C. | C(Na+)═2[c(HCO3-)+c(CO32-)+c(H2CO3)] | D. | C(OH-)═c(HCO3-)+c(H+)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | L是极性分子,G是非极性分子 | |
| B. | M分子中含2个π键和1个σ键 | |
| C. | E极易溶于水的原因是与水分子形成氢键 | |
| D. | E分子中键角为104.5° |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液溴和苯分别受热变为气体 | B. | 干冰和氣化铵分别受热变为气体 | ||
| C. | 氧化硅和铁分别受热熔化 | D. | 食盐和葡萄糖分别溶解在水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
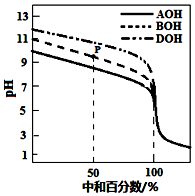 室温下,用相同物质的量浓度的HCl溶液,分别滴定物质的量浓度均为0.1mol•L-1的三种碱(AOH、BOH和DOH)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同物质的量浓度的HCl溶液,分别滴定物质的量浓度均为0.1mol•L-1的三种碱(AOH、BOH和DOH)溶液,滴定的曲线如图所示,下列判断正确的是( )| A. | 滴定时,随着盐酸溶液的滴入,水电离出的c(H+)始终增大 | |
| B. | 滴定至P点时,溶液中:c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+) | |
| C. | pH=7时,三种溶液中c(Cl-) 相等 | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示.
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com