
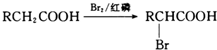
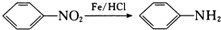 (-NH2易被氧化)
(-NH2易被氧化) 、
、 .
.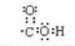 .H的化学名称为对硝基甲苯.
.H的化学名称为对硝基甲苯. $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$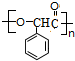 +nH2O.
+nH2O.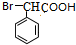 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$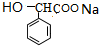 +NaBr+H2O.
+NaBr+H2O.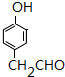 .
. 的合成路线CH3CH2CH2OH$→_{催化剂}^{氧气}$CH3CH2CHO$→_{催化剂}^{氧气}$CH3CH2COOH$\stackrel{溴/红磷}{→}$CH3CHBrCOOH$\stackrel{氢氧化钠醇溶液}{→}$CH2=CHCOOH$→_{△}^{甲醇/浓H_{2}SO_{4}}$CH2=CHCOOCH3$\stackrel{催化剂}{→}$
的合成路线CH3CH2CH2OH$→_{催化剂}^{氧气}$CH3CH2CHO$→_{催化剂}^{氧气}$CH3CH2COOH$\stackrel{溴/红磷}{→}$CH3CHBrCOOH$\stackrel{氢氧化钠醇溶液}{→}$CH2=CHCOOH$→_{△}^{甲醇/浓H_{2}SO_{4}}$CH2=CHCOOCH3$\stackrel{催化剂}{→}$ (无机试剂任选).
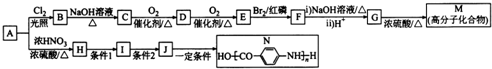
(无机试剂任选).分析 芳香烃A的蒸汽密度是同条件下H2密度的53倍,所以其相对分子质量为106,令分子组成为CxHy,则$\frac{106}{12}$=8…10,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃A的分子式为C8H10,其结构简式为 ,根据各物质的转化关系,A与氯气在光照条件下发生取代反应生成B为
,根据各物质的转化关系,A与氯气在光照条件下发生取代反应生成B为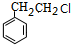 ,B与氢氧化钠溶液发生水解生成C为
,B与氢氧化钠溶液发生水解生成C为 ,C催化氧化生成D为
,C催化氧化生成D为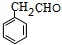 ,D氧化生成E为
,D氧化生成E为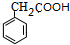 ,E与溴发生信息③中的取代反应生成F为
,E与溴发生信息③中的取代反应生成F为 ,F发生水解生成G为
,F发生水解生成G为 ,G发生缩聚反应得M为
,G发生缩聚反应得M为 ,A与浓硫酸、浓硝酸发生硝化反应得H为
,A与浓硫酸、浓硝酸发生硝化反应得H为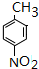 ,H发生氧化反应生成I为
,H发生氧化反应生成I为 ,I发生还原反应生成J为
,I发生还原反应生成J为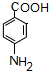 ,J发生缩聚反应得N,以CH3CH2CH2OH和CH3OH为原料制备
,J发生缩聚反应得N,以CH3CH2CH2OH和CH3OH为原料制备 ,可以将CH3CH2CH2OH氧成CH3CH2COOH,再用CH3CH2COOH与溴发生取代反应生成CH3CHBrCOOH,CH3CHBrCOOH发生消去后与甲醇酯化再加聚可得产品,据此答题;
,可以将CH3CH2CH2OH氧成CH3CH2COOH,再用CH3CH2COOH与溴发生取代反应生成CH3CHBrCOOH,CH3CHBrCOOH发生消去后与甲醇酯化再加聚可得产品,据此答题;
解答 解:芳香烃A的蒸汽密度是同条件下H2密度的53倍,所以其相对分子质量为106,令分子组成为CxHy,则$\frac{106}{12}$=8…10,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃A的分子式为C8H10,其结构简式为 ,根据各物质的转化关系,A与氯气在光照条件下发生取代反应生成B为
,根据各物质的转化关系,A与氯气在光照条件下发生取代反应生成B为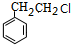 ,B与氢氧化钠溶液发生水解生成C为
,B与氢氧化钠溶液发生水解生成C为 ,C催化氧化生成D为
,C催化氧化生成D为 ,D氧化生成E为
,D氧化生成E为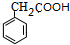 ,E与溴发生信息③中的取代反应生成F为
,E与溴发生信息③中的取代反应生成F为 ,F发生水解生成G为
,F发生水解生成G为 ,G发生缩聚反应得M为
,G发生缩聚反应得M为 ,A与浓硫酸、浓硝酸发生硝化反应得H为
,A与浓硫酸、浓硝酸发生硝化反应得H为 ,H发生氧化反应生成I为
,H发生氧化反应生成I为 ,I发生还原反应生成J为
,I发生还原反应生成J为 ,J发生缩聚反应得N,
,J发生缩聚反应得N,
(1)根据上面的分析可知,A为 ,I为
,I为 ,
,
故答案为: ;
; ;
;
(2)F为 ,F中含氧官能团为羧基,其电子式为
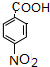
,F中含氧官能团为羧基,其电子式为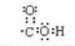 ,H为
,H为 ,H的化学名称为对硝基甲苯,
,H的化学名称为对硝基甲苯,
故答案为: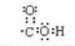 ;对硝基甲苯;
;对硝基甲苯;
(3)根据上面的分析可知,C→D的反应类型为氧化反应,J→N的反应类型为缩聚反应,
故答案为:氧化反应;缩聚反应;
(4)G→M的化学方程式为n $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +nH2O,
+nH2O,
F为 ,加热条件下,F与足量NaOH溶液反应的化学方程式为
,加热条件下,F与足量NaOH溶液反应的化学方程式为 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +NaBr+H2O,
+NaBr+H2O,
故答案为:n $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +nH2O;
+nH2O; +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +NaBr+H2O;
+NaBr+H2O;
(5)E为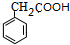 ,E的同分异构体中,既能发生银镜反应又能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,则符合条件的结构为苯环上连有-CH3、-OH、-CHO,有10种结构,或为苯环上连有-CH2CHO、-OH,有3种结构,所以共有13种,其中核磁共振氢谱有5种吸收峰,且峰面积之比为1:2:2:2:1的结构简式为
,E的同分异构体中,既能发生银镜反应又能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,则符合条件的结构为苯环上连有-CH3、-OH、-CHO,有10种结构,或为苯环上连有-CH2CHO、-OH,有3种结构,所以共有13种,其中核磁共振氢谱有5种吸收峰,且峰面积之比为1:2:2:2:1的结构简式为  ,
,
故答案为:13; ;
;
(6)以CH3CH2CH2OH和CH3OH为原料制备 ,可以将CH3CH2CH2OH氧成CH3CH2COOH,再用CH3CH2COOH与溴发生取代反应生成CH3CHBrCOOH,CH3CHBrCOOH发生消去后与甲醇酯化再加聚可得产品,反应的合成路线为CH3CH2CH2OH$→_{催化剂}^{氧气}$CH3CH2CHO$→_{催化剂}^{氧气}$CH3CH2COOH$\stackrel{溴/红磷}{→}$CH3CHBrCOOH$\stackrel{氢氧化钠醇溶液}{→}$CH2=CHCOOH$→_{△}^{甲醇/浓H_{2}SO_{4}}$CH2=CHCOOCH3$\stackrel{催化剂}{→}$
,可以将CH3CH2CH2OH氧成CH3CH2COOH,再用CH3CH2COOH与溴发生取代反应生成CH3CHBrCOOH,CH3CHBrCOOH发生消去后与甲醇酯化再加聚可得产品,反应的合成路线为CH3CH2CH2OH$→_{催化剂}^{氧气}$CH3CH2CHO$→_{催化剂}^{氧气}$CH3CH2COOH$\stackrel{溴/红磷}{→}$CH3CHBrCOOH$\stackrel{氢氧化钠醇溶液}{→}$CH2=CHCOOH$→_{△}^{甲醇/浓H_{2}SO_{4}}$CH2=CHCOOCH3$\stackrel{催化剂}{→}$ ,
,
故答案为:CH3CH2CH2OH$→_{催化剂}^{氧气}$CH3CH2CHO$→_{催化剂}^{氧气}$CH3CH2COOH$\stackrel{溴/红磷}{→}$CH3CHBrCOOH$\stackrel{氢氧化钠醇溶液}{→}$CH2=CHCOOH$→_{△}^{甲醇/浓H_{2}SO_{4}}$CH2=CHCOOCH3$\stackrel{催化剂}{→}$ .
.
点评 本题考查有机物的推断与合成,难度中等,关键是利用A的相对分子质量推断A的结构,结合B的反应产物的C可以连续发生氧化反应判断B的结构,再根据反应条件及反应信息进行判断,是对有机物知识的综合考查,能较好的考查学生的分析思维能力,是有机热点题型.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 44gCO2和N2O的混合物中含有的氧原子数为1.5NA | |
| B. | 2L0.5mol/L亚硫酸氢钠溶液中含有的HSO3-离子数为NA | |
| C. | 氢氧化钠与氯气反应时,生成0.1molNaCl转移的电子数为0.1NA | |
| D. | 一定条件下在密闭容器中2molSO2与2molO2充分反应,最终的气体分子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
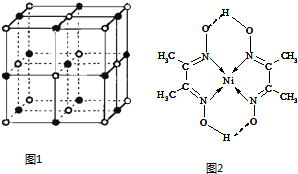
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的pH一定等于1 | |
| B. | 阴离子肯定有I-,不能确定有无HCO${\;}_{3}^{-}$ | |
| C. | 阳离子肯定没有Fe3+,一定有Na+ | |
| D. | 该溶液含有的溶质成分可能为HI;或HI和NaI;或NaI和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 配制FeCl3溶液时,加入适量盐酸 | 增大Cl-浓度,可以抑制Fe3+水解 |
| B | Cl2通入人品红溶液中,品红褪色 | Cl2具有漂白性 |
| C | 久置的漂白粉质量减小 | 漂白粉中的Ca(ClO)2转化为CaCO3 |
| D | AgI可用于人工降雨 | AgI气化时吸热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢化玻璃的成分与普通玻璃一样,有机玻璃是聚合物 | |
| B. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 | |
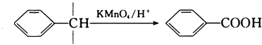
| C. | 苹和甲苯互为同系物,均能使KMnCL4酸性溶液褪色 | |
| D. | 按系统命名法,化合物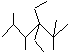 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
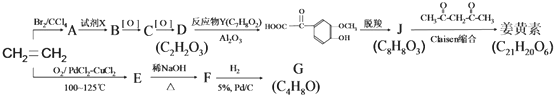
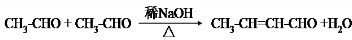 ,F 到 G 的反应类型加成反应或还原反应
,F 到 G 的反应类型加成反应或还原反应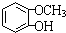 ,姜黄素的结构简式
,姜黄素的结构简式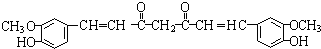
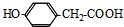 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

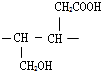 ;
;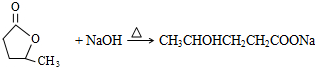 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤操作中,漏斗的尖端应接触烧杯内壁 | |
| B. | 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 | |
| C. | 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 | |
| D. | 向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com