
| | ¢Ł | ¢Ś | ¢Ū | ¢Ü |
| ČÜŅŗ | °±Ė® | ĒāŃõ»ÆÄĘČÜŅŗ | “×Ėį | ŃĪĖį |
| pH | 11 | 11 | 3 | 3 |


 ŗčĶ¼Ķ¼Źéŗ®¼Ł×÷Ņµ¼ŁĘŚ×÷Ņµ¼ŖĮÖ“óѧ³ö°ęÉēĻµĮŠ“š°ø
ŗčĶ¼Ķ¼Źéŗ®¼Ł×÷Ņµ¼ŁĘŚ×÷Ņµ¼ŖĮÖ“óѧ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®10 mL 0.1 mol”¤L-1ŃĪĖį£¬c£ØCl-£©£¾c(OH-)£¾c(H+) |
B£®10 mL 0.1 mol”¤L-1°±Ė®£¬c(OH-)£¾c( )£¾c(H+) )£¾c(H+) |
| C£®5 mL 0.2 mol”¤L-1NaOHČÜŅŗ£¬c(Na+)£¾c(OH-)£¾c(H+) |
| D£®10 mL 0.5 mol”¤L-1NaOHČÜŅŗÓė6 mL 1 mol”¤L-1ŃĪĖį»ģŗĻ£¬c(Cl-)£¾c(Na+)£¾c(OH-)£¾c(H+) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®MgCO3ÓėŃĪĖį·“Ó¦£ŗCO32-+2H+ ="=" CO2”ü+H2O |
| B£®Mg(OH)2ÓėH2SO4·“Ó¦£ŗMg2++2OH-+2H++SO42- ="=" MgSO4”ż+2H2O |
| C£®Ć¾Óė“×Ėį·“Ó¦£ŗMg+2H+ ="=" Mg2++H2”ü |
| D£®¹¤ŅµÉĻŅŌŗ£Ė®ĪŖŌĮĻÖʱøMg(OH)2£ŗCa(OH)2+Mg2+ ="=" Mg(OH)2”ż+Ca2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ś¢Ü | B£®¢Ł¢Ś¢Ü | C£®¢Ł¢Ū¢Ü | D£®¢Ł¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 Ag£«(aq)£«Cl£(aq)
Ag£«(aq)£«Cl£(aq)²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®c(OH-)/c(H+)=1010µÄČÜŅŗ£ŗK+”¢Fe3+”¢Cl-”¢NO3- |
| B£®ÄÜÉś³ÉAl(OH)3µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢ClO-”¢SO32- |
| C£®ÄÜŹ¹·ÓĢŖ±äŗģµÄČÜŅŗ£ŗNa+”¢Ba2+”¢NO3-”¢I- |
| D£®³ĪĒåĶøĆ÷µÄĪŽÉ«ČÜŅŗ£ŗNH4+”¢K+”¢MnO4-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| ČõĖįµÄ»ÆѧŹ½ | CH3COOH | HCN | H2CO3 |
| µēĄėĘ½ŗā³£Źż(25”ę) | 1.8”Į10£5 | 4.9”Į10£10 | K1£½4.3”Į10£7 K2£½5.6”Į10£11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Na£«”¢Mg2£«”¢Cl£”¢OH£ | B£®H£«”¢Ca2£«”¢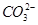 ”¢ ”¢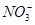 |
C£®Cu2£«”¢K£«”¢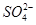 ”¢ ”¢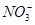 | D£®Na£«”¢H£«”¢OH£”¢Ca2£« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®HCO3Ņ» | B£®Ba2+ | C£®Al3+ | D£®Ag+ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com